硅油在工业上通常称为硅油或硅酮,化学结构是聚二甲基硅氧烷(PDMS),以三甲基硅氧烷氧基为端基,其中二甲基硅氧烷单元的数量决定了硅酮的分子量和粘度。
硅油作为优良润滑剂,广泛应用于药品包装组件中,以改善其加工性和/或功能性,例如用于橡胶塞生产中的硅化过程,以及预注射器的玻璃针管,确保活塞顺畅滑动于针管内。
然而,尽管硅油具有良好的物理化学性能,但其疏水性和在溶剂中的溶解性,对生物制品可能产生潜在影响。特别是对于抗体或蛋白类药物而言,如单克隆抗体(Mab)和融合蛋白药物,硅油与蛋白界面的接触使得蛋白更易发生变性和聚集。
多项研究表明蛋白质的表面性质、界面性质和溶液条件都会影响其与硅油的亲和力和相互作用程度。
硅油和蛋白之间的相互作用机制以及影响因素又是什么?
这对理解生物制品在包装组件中的稳定性有很大意义。带着这样的问题进行探讨,相信对生物类产品的开发和生产有着一定意义,我们才能有效减少硅油对蛋白类药物的不良影响。
|相互作用机制
控制蛋白质分子与界面相互作用的两种主要作用力是静电作用力和疏水作用力。取决于构成蛋白质分子的氨基酸的pka值和溶液pH,蛋白质将被电离到不同程度而携带电荷。如果界面上的基团具有电离能力,也会带电,蛋白质分子可以通过相反电荷之间的静电相互作用与界面结合。当界面不带电且非极性时,疏水作用主要驱动吸附过程。
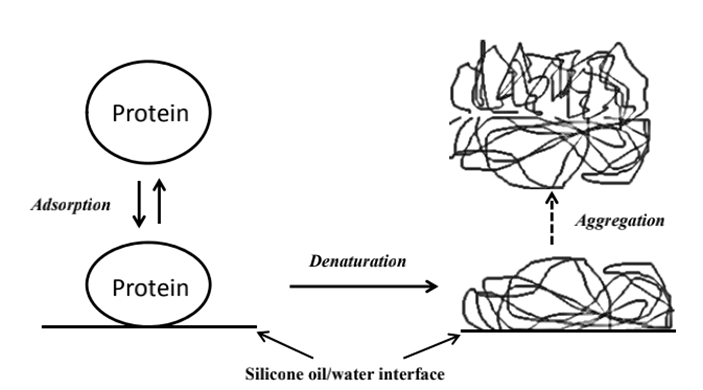 图1 蛋白质在硅油/水界面上的吸附和聚集
图1 蛋白质在硅油/水界面上的吸附和聚集
| 关键影响因素
影响蛋白质吸附的因素包括:蛋白质的表面和结构性质、界面和溶液条件,具体如下:
-
蛋白质:分子大小、表面电荷、疏水性和结构稳定性;
-
界面:疏水性和表面电荷主导因素;
-
溶液条件:蛋白质浓度、pH值、离子强度和赋形剂;
现就以上的因素逐一进行分析。
蛋白质结构稳定性的影响:高结构稳定性蛋白(硬蛋白,刚性蛋白)只有在静电有利时才会吸附到带电表面。软低结构稳定性蛋白(软蛋白,柔性蛋白)即使在静电排斥的条件下也会被吸附,蛋白质分子在界面处结构变化会导致系统熵的大幅增加,驱动蛋白质在疏水界面的吸附。
蛋白质表面电荷的影响:增加蛋白质分子表面的净电荷使得被吸附分子之间的电荷排斥将增加,可能会减少其对界面的吸附。另外随着净电荷的增加,由于分子内排斥力,蛋白质分子的构象可能会更为延伸,这可能会导致吸附量减少。
蛋白质浓度的影响:蛋白质的浓度对界面上蛋白质的吸附量有影响,这可以通过吸附等温线来说明。在不同的疏水界面上,蛋白质吸附在低体积蛋白质浓度下急剧上升,随后在高浓度下趋于平稳。可以采用Langmuir、Freundlich、random sequential等模型拟合蛋白在界面吸附。
溶液离子强度的影响:盐通常添加到蛋白质制剂中,以调节溶液张力并保持制剂离子强度。如果蛋白质在特定条件下带有净表面电荷,那么在疏水界面上,增加离子强度将增加吸附量。然而这种效应取决于蛋白质和界面种类,不同离子强度下不同蛋白对界面吸附的影响应异。
pH值:蛋白质吸附是熵驱动的,吸附量在等电点附近出现最大值。这是因为在等电点,分子具有更球状的构型,而对于较小和较大的pH值,分子内静电斥力导致更广泛的构型。因此,在等电点,蛋白质分子吸附所需的表面相邻位点的数量最小,因此吸附的可能性最大。
此外,对于不同于等电点的pH值,被吸附的蛋白质分子产生排斥性静电相互作用,从而减缓进一步的吸附。
|预灌封注射器(PFS)
预灌封注射器由于其使用的便捷性、给药体积准确性、使用安全性等优势,广泛应用于生物制品、生化类产品、抗血栓药、美容产品等高产值产品的包装。
可以考虑通过以下几个方面减少硅油的不良影响。
工艺优化
预灌封注射器玻璃针筒硅化过中需要控制的参数包括泵和喷嘴设置、喷雾量和速率、硅乳液浓度、通道温度、通道长度和通道暴露时间等。
预灌封注射器制造商已经设计了一些工艺(如“烘焙”)以获得物理稳定的硅油涂层,使用粘度较高的硅油等级提高表面硅油膜的物理稳定性,使用潜水喷嘴可获得更均匀的涂层等。
配方改进
可在配方中添加非离子表面活性剂。在药物配方中使用非离子表面活性剂可将吸附降至最低。
在生物制药中使用表面活性剂以达到稳定效果的主要原因是:(1)表面活性剂与蛋白竞争共同界面;(2)表面活性剂通过疏水位点与蛋白相互作用,以防止蛋白的潜在表面吸附。
研究表明吐温®20在固体硅油/水界面上的吸附以松散填充的单层模式发生,与同一界面上的结合蛋白相比,结合表面活性剂层具有显著更大的粘性,可有效地显著降低蛋白对表面活性剂的吸附。但是目前对表面活性剂在影响蛋白-硅油相互作用中的作用仍缺乏深入了解。
替代产品
开发塑料等替代材料,由环烯烃聚合物(COP)或共聚物(COC)制成的预灌封注射器(例如BD Sterifill SCF™,山东威高、Gerresheimer等)。
市场上第一个无硅油润滑的注射器系统是West Daikyo CZ®是长插入式针头注射器系统,注射器筒由Daikyo专有的Crystal Zenith制造的环烯烃聚合物,其活塞带Daikyo的FluroTec®涂层(四氟乙烯(EFTE)和乙烯的共聚物膜),无需硅酮即可保证活塞的滑动性。环烯烃注射器虽然具有透明、重量轻、不易破碎或低金属离子浸出等优点,但对氧气和水的渗透性更强,氧气在储存期间的渗透可能对氧化敏感蛋白有害。
|结论
硅油的存在可能导致包材与蛋白类药物不相容,但无法建立一般规则。一些蛋白在接触硅油后立即出现不良反应,而另一些蛋白在较长时间内并没有表现出任何不稳定性。
硅油的不良影响依赖于蛋白质本身的特性如疏水性和结构稳定性,在聚集过程中涉及不同的动力学。因此,需要对硅油对蛋白的影响进行个案评估。目前仍然缺乏关于其界面机制的知识,深入研究蛋白在硅油/水界面上的长期吸附-解吸行为有助于设计更稳定的产品,用于蛋白-底物相互作用的表征的高灵敏度技术包括椭偏仪、石英晶体微天平(QCM)、表面等离子体共振(SPR)、全内反射荧光成像(TIRF)、X射线光电子能谱(XPS)等可供选择。
|结束语
尽管硅油由于其良好的物理化学性质和生物相容性作为润滑剂被广泛使用,然而其疏水性和在药物溶液中浸出的倾向是生物制药存储需要考虑的一个问题。
尽管硅油不一定对所有蛋白类药物都有不良影响,但在选择包装材料时,需要综合考虑蛋白本身的特性、溶液性质和界面特性等多方面因素。
总的来说,深入研究硅油与不同蛋白之间的复杂相互作用机制,对减少其不良作用至关重要。其中关键是需要理解不同蛋白对硅油的敏感性差异,寻求定制化解决方案,这期待行业持续进步与各方合作的不断加强。
参考文献:
- Investigation of Factors Affecting Protein-Silicone Oil Interactions,Nitin Dixit, Ph.D. 2013.
- Mizutani T 1981. Estimation of protein and drug adsorption onto silicone-coated glass surfaces. J Pharm Sci. 1981,70(5):493-496.
- Li J, Pinnamaneni S, Quan Y, Jaiswal A, Andersson F, Zhang X, Mechanistic understanding of protein-silicone oil interactions. Pharm Res. 2012, 29(6):1689-1697.
- Fries A. Drug delivery of sensitive biopharmaceuticals with prefilled syringes. Drug Delivery Technol. 2009, 9(5):22, 24-27.
- Jones LS, Kaufmann A, Middaugh CR. Silicone oil induced aggregation of proteins. J Pharm Sci. 2005, 94(4):918-927.
- Luey JK, McGuire J, Sproull RD. The effect of pH and sodium chloride concentration on adsorption of β-lactoglobulin at hydrophilic and hydrophobic silicon surfaces. J Colloid Interface Sci. 1991, 143(2):489-500.
- Dixit N, Maloney KM, Kalonia DS. The effect of Tween® 20 on silicone oil– fusion protein interactions. Int J Pharm. 2012, 429(1–2):158-167.
- Thirumangalathu R, Krishnan S, Ricci MS, Brems DN, Randolph TW, Carpenter JF. Silicone oil- and agitation-induced aggregation of a monoclonal antibody in aqueous solution. J Pharm Sci. 2009, 98(9):3167-3181.