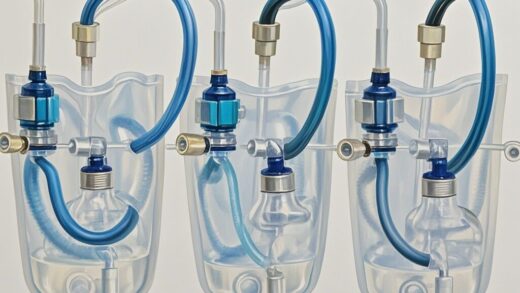
默沙东的Keytruda(帕博利珠单抗)已经是全球销售额最高的药物,2024年全年销售额达到294亿美元(约合人民币210亿元),同比增长18%。这个数字背后,是PD-1/PD-L1抑制剂市场的持续扩张,也是生物制药行业供应链的一场深刻变革。当一款药物的年销售额逼近300亿美元,它的每一个生产环节都变成了一个产业。从细胞培养到纯化,从制剂灌装到最终包装,一次性生物工艺组件贯穿其中。本文将围绕Keytruda的市场表现与适应症拓展,梳理其产业链对一次性工艺组件的拉动逻辑,并分析这一趋势对制药企业供应链策略的启示。
一款200亿级药物的生长轨迹
Keytruda的故事开始于2014年获批上市,但它的爆发期集中在近五年。2019年销售额首次突破100亿美元,2021年达到171亿美元,2023年突破250亿美元,2024年逼近300亿美元。这种指数级增长并非来自单一市场的饱和,而是不断拓展的适应症地图。截至目前,Keytruda已在全球获批用于超过40种适应症,覆盖黑色素瘤、非小细胞肺癌、肾细胞癌、头颈鳞癌、霍奇金淋巴瘤、微卫星不稳定性高(MSI-H)实体瘤等多个瘤种,并持续向早期肿瘤治疗、新辅助治疗和辅助治疗阶段延伸。2024年,Keytruda又在子宫内膜癌、肝细胞癌等新适应症上获得监管批准,进一步扩大了患者基数。
这种适应症的拓展直接转化为生产规模的扩张。一款单克隆抗体的商业化生产,通常需要数千升至数万升的细胞培养规模。Keytruda作为全人源化IgG4单克隆抗体,其生产工艺高度标准化,但产量需求随着适应症的拓展呈倍数增长。据行业估算,单个2000L一次性生物反应器批次大约可产出80-120kg的抗体原液。假设Keytruda在全球的年需求量达到数吨级别,那么仅细胞培养环节就需要数十甚至上百个批次的不锈钢或一次性反应器运行。这还不包括下游纯化、过滤、制剂灌装等环节对一次性组件的需求。
适应症拓展背后的产能焦虑
Keytruda适应症拓展带来的不仅是用药人群的增加,还有用药方案的变化。近年来,Keytruda在多个癌种中获批与化疗的联合治疗方案,这意味着给药剂量的调整和用药频次的增加。某些适应症中,Keytruda的使用周期从每三周一次延伸至长期用药,患者的平均治疗时长显著增加。这种用药方案的演变,使得单位患者所需的药物产量进一步提升,制药企业面临的产能压力随之加剧。
对于默沙东这样的跨国药企而言,解决产能问题主要有两条路径:一是自建或扩建不锈钢生物反应器产能,二是依赖一次性工艺技术快速提升灵活性。两条路径并非互斥,许多企业选择并行推进。但在实际操作中,新建不锈钢产能的资本支出动辄数亿美元,且建设周期长达三到五年。相比之下,一次性生物工艺组件的部署周期短、初始投入相对可控,且在面对市场需求波动时可以灵活调整产能。默沙东在全球多个生产基地布局了包括一次性生物反应器、一次性超滤系统、一次性制剂灌装线在内的综合工艺体系,这已成为行业内的通行做法。
这种产能策略的底层逻辑在于:生物制药行业的需求波动性正在加剧。一款重磅药物可能在专利到期前面临仿制药竞争,而新的适应症拓展又会带来阶段性的需求峰值。一次性工艺组件的可扩展性和灵活性,恰好契合了这种“快速响应、弹性生产”的需求。全球范围内,采用一次性技术进行商业化抗体生产的企业比例在过去五年中从不足20%提升至超过40%,这一趋势在Keytruda等大品种的带动下仍在加速。
一次性生物工艺组件的品类需求图谱
Keytruda的生产链条对一次性工艺组件的需求,可以沿着上游细胞培养、下游纯化和制剂灌装三个环节来拆解。
在上游细胞培养环节,一次性生物反应器是最核心的组件。从50L规模的种子培养到2000L甚至4000L的商业化规模培养,一次性波浪式反应器和搅拌式生物反应器(如ABDK、UniVessel SU等型号)在抗体生产中广泛应用。这些反应器内袋、培养基储袋、补料袋等耗材与产品直接接触,其材质选择、溶出物水平和生物相容性直接影响细胞培养的表现和最终产品质量。Keytruda作为高产量抗体,其培养过程中对培养基消耗量极大,培养基储袋和液体传输组件的单批使用量远超普通品种。
在下游纯化环节,一次性组件的渗透同样深入。Protein A亲和层析仍是单克隆抗体纯化的核心步骤,虽然层析填料本身通常为反复使用的固相介质,但层析系统的管路、阀门、泵头、收集器等部件已大量采用一次性设计。超滤/渗滤(UF/DF)步骤中的膜包、滤芯、配液袋、传输管路同样高度依赖一次性组件。Keytruda的下游纯化需要处理大量细胞培养上清液,对过滤组件的通量和载量提出了严苛要求。一次性深层过滤器、0.22μm终端过滤器和除病毒过滤器的消耗量随产量线性增加。
制剂灌装环节是一次性工艺组件应用最为密集的阶段。从原液稀释、缓冲液配制到最终灌装,几乎所有与产品接触的液体路径都已实现一次性化。一次性灌装针头、蠕动泵管路、灌装管、冻存袋、西林瓶胶塞和铝盖的灭菌托盘等组件构成了完整的无菌灌装体系。Keytruda作为注射剂型,对无菌保障的要求极高,制剂灌装线的每一个环节都必须在严格的GMP条件下运行,这对一次性组件的供应商资质和产品质量提出了更高标准。
值得注意的是,除了上述三个核心环节,一次性取样系统、一次性袋子(用于原液储存和运输)、一次性焊接设备等辅助组件同样构成了Keytruda产业链中不可或缺的配套环节。尤其是Keytruda的全球供应涉及跨境运输,原液和制剂的冷链储运对一次性冻存袋和保温运输箱的需求量极大。这些看似“配角”的组件,在整个供应链中占据的成本比例正在持续上升。
供应链上游的审评合规压力
Keytruda的全球供应网络跨越多个生产基地和监管辖区,其供应链上游的一次性组件供应商面临着极为严格的审评合规要求。美国FDA、欧盟EMA以及中国国家药品监督管理局对生物制药生产中使用的一次性组件均有明确的法规框架。在美国药典(USP)层面,USP<661>对塑料包装材料、USP<665>对生物制药生产中使用的塑料和聚合物组件、USP<1665>对生物制药一次性系统均有专门论述。欧洲药典(EP)则在3.1节系列中对塑料原材料进行了详细规定。ICH Q3E指南体系则从可提取物和可浸出物(E&L)角度,对组件与药物接触时的安全性评估提供了科学框架。
这一合规体系的严格程度,在Keytruda这样的明星药物上体现得尤为突出。药品监管机构不仅关注最终制剂的质量,对生产过程中使用的每一种接触材料的安全性同样进行审查。对于Keytruda这类年销售额数百亿美元的产品,任何与材料相关的质量事件都可能引发产品召回或供应中断,其风险成本远超组件本身的采购价值。因此,制药企业在选择一次性组件供应商时,供应商的质量管理体系、变更控制能力、E&L研究数据完整性以及 Regulatory Support 能力均成为关键考量因素。
具体到E&L研究层面,一次性生物反应器内袋、培养基储袋、配液袋等与细胞培养液直接接触的组件,其可提取物谱的鉴定和可浸出物风险评估是药品上市前必须完成的研究工作。Keytruda的生产工艺变更,包括但不限于关键耗材供应商的变更,必须按照FDA的PAI(批准前检查)和NDA/NBEs补充申请流程进行申报。2022年,默沙东曾就Keytruda多个规格的补充申请提交变更,涉及其生产工艺中某些耗材的供应商调整,这一过程要求提供详实的可浸出物数据和安全性评估报告。
我们在实际项目中观察到,越来越多的大型生物制药企业在选择一次性组件供应商时,倾向于选择能够提供一站式E&L研究服务和 Regulatory Package 的合作伙伴。伯朗氏实验室在为客户进行一次性生产组件的相容性研究时发现,组件供应商提供的标准 E&L数据包与企业特定制剂条件之间往往存在差距——不同产品的溶剂体系、接触时间、温度和灭菌方式都会影响浸出物的种类和量级。这意味着,制药企业需要针对自身产品进行定制化的可浸出物研究,而非简单依赖供应商的通用数据模板。
市场增量与竞争格局的再平衡
Keytruda的适应症拓展仍在继续。2025年初,Keytruda在新辅助治疗三阴性乳腺癌和早期肝细胞癌辅助治疗领域获得了新的监管批准,进一步扩大了适用人群。PD-1/PD-L1抑制剂市场的整体规模预计将在2030年突破600亿美元,而Keytruda凭借先发优势和广泛的适应症布局,仍将占据最大市场份额。这意味着围绕Keytruda产业链的一次性工艺组件需求,将在未来数年保持持续增长。
竞争格局方面,百时美施贵宝的Opdivo曾与Keytruda形成双雄争霸局面,但Opdivo近年来的销售额增长明显放缓,与Keytruda的差距逐渐拉大。阿斯利康的Imfinzi、罗氏的Tecentriq、葛兰素史克的Jemperli等后续竞争者各自占据细分适应症市场,但整体市场份额仍高度集中于Keytruda。这种“一超多强”的市场格局,决定了Keytruda产业链的供应链决策对整个行业具有示范效应。
从生物工艺组件供应商的角度观察,Keytruda的供应链体系主要由Cytiva、Sartorius、Merck Millipore、Thermo Fisher Scientific、Sealed Air等国际厂商提供核心组件。这些厂商在一次性生物反应器、过滤系统、储液配液系统等领域的占有率极高。但值得关注的是,中国本土的一次性工艺组件供应商在过去三年中取得了显著进展。部分国内厂商的细胞培养袋、储液袋、过滤产品已进入国内头部生物制药企业的商业化生产线,虽然在高端应用场景(如大规模商业化制剂灌装)的渗透率仍相对有限,但增长势头明确。
对于国内生物制药企业而言,Keytruda的案例提供了双重启示:一方面,它验证了重磅品种如何通过适应症拓展持续放大产业规模,进而带动上游供应链的繁荣;另一方面,它也提醒企业从早期工艺开发阶段就需要建立稳健的耗材供应商管理体系,尤其是在一次性组件的合规性评估和供应链韧性建设方面。
给制药企业的行动建议
基于上述分析,我们对制药企业在一次性生物工艺组件领域的策略提出几点建议。首先,在早期工艺开发阶段就应当将耗材的合规性纳入考量,而非在商业化前夕被动应对。一套完整的一次性组件 E&L 评估和药包材相容性研究方案,通常需要三到六个月的项目周期,如果企业能够在工艺设计阶段就启动相关研究,将显著降低后期变更的风险和成本。
其次,供应链多元化是应对地缘政治和突发事件的关键能力。单一供应商依赖在大规模商业化生产中是风险极高的策略。我们建议企业针对关键耗材(如一次性生物反应器内袋、终端过滤器、灌装组件)建立至少两家合格供应商,并通过定期审计和变更控制确保供应链的持续合规。
再次,关注一次性组件的可持续发展趋势。生物制药行业对一次性塑料废弃物问题的关注度正在提升。Sartorius、Cytiva等头部厂商已推出减少塑料用量的优化设计,部分企业开始探索可重复使用组件与一次性组件的混合工艺路线。从长期看,组件的可回收性和低碳设计将逐渐成为供应商选择的重要维度。
对于正在布局生物药管线或计划拓展现有抗体药物适应症的企业,我们建议尽早与具备 E&L 研究能力和 USP/ICH Q3E 合规评估经验的专业实验室建立合作。伯朗氏实验室能够为制药企业提供一次性生产组件的可提取物与可浸出物研究、药包材相容性评估、以及针对特定产品和工艺条件的定制化合规方案,帮助企业在供应链管理的上游就把控质量和合规风险。
免责声明:本文所引用数据来源于公开行业报告、FDA审批文件和公司年报,部分市场数据为基于已知信息的合理估算。文中涉及的商业化生产信息属于行业常识范畴,不涉及任何厂商的商业机密。具体数据和案例仅供行业分析参考,不构成投资建议。企业在实际决策中应结合自身情况并咨询专业顾问。
参考来源:Merck & Co. Annual Report 2024;EvaluatePharma World Preview 2024;FDA药物审批数据库;USP <661>, <665>, <1665>;ICH Q3E (E&L) 相关指南文件;BioPlan Associates 《全球生物工艺耗材市场报告》2024。