1. 引言
1.1 背景
药品的纯度对于药品的安全性、质量和有效性至关重要。药品中检出的杂质应得到充分鉴定,并对其毒理学风险进行评估。在药品中最常遇到的杂质包括活性成分或辅料的降解产物、可浸出物和迁移物。其中,可浸出物(Leachables)和迁移物(Migrants)属于外源性化学实体。
可浸出物是指在储存或使用过程中从包装系统浸入已包装药品的化合物[1]。可浸出物通常来源于生产接触表面(生产设备)或药品包装(初级和次级包装),因直接接触而产生。迁移物则被描述为在穿透物理屏障(如初级包装所提供的屏障)后在药品中积累的化合物[2]。
1.2 滴眼剂包装概述
滴眼剂是临床常用的眼用制剂,其包装形式主要为塑料滴眼剂瓶。市场上常见的滴眼剂瓶材质包括:
| 材质 | 特性 | 典型应用 |
|---|---|---|
| LDPE(低密度聚乙烯) | 柔软、弹性好,便于挤压给药 | 大多数眼用液体制剂 |
| PP(聚丙烯) | 刚性较好,耐高温,阻隔性能优于LDPE | 需高温灭菌的滴眼剂 |
| COP/COC(环烯烃聚合物/共聚物) | 优良的光学性能和化学耐受性 | 高端眼用制剂 |
本研究所涉及的滴眼剂采用LDPE瓶身配PP螺旋盖的组合包装形式。
1.3 印刷标签中的松香基组分
印刷标签作为次级包装的重要组成部分,其印刷油墨和粘合剂中含有多种有机化合物。松香及其衍生物是印刷油墨中常用的粘合组分和增粘剂,在凸版印刷、柔版印刷和胶印油墨中均有广泛应用。
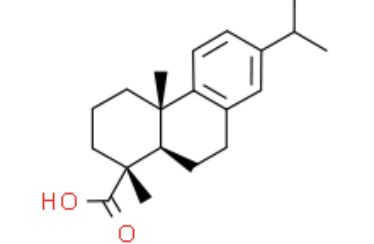
脱氢松香酸(Dehydroabietic Acid, DHAA)是松香的主要活性成分之一,属于树脂酸类化合物。松香中的树脂酸组分包括松香酸(约40-50%)、左旋海松酸(约15-25%)、去氢枞酸/脱氢松香酸(约10-15%)以及其他微量树脂酸[3]。
DHAA已被报道具有皮肤致敏性和细胞毒性[4,5],其在药品中的存在应引起高度重视。本案例旨在阐明DHAA从标签向滴眼剂迁移的风险,并明确其来源属性。
2. 材料与方法
2.1 化学品与材料
分析纯级甲酸、乙酸铵购自Fisher Scientific公司(美国)。HPLC级甲醇、乙腈购自Fisher Scientific公司。脱氢松香酸标准品(纯度≥98%)购自Sigma-Aldrich公司(美国)。实验用水由MilliQ纯水系统(Millipore,法国)制备。
某滴眼剂(规格:5 mL/瓶,LDPE滴眼剂瓶配PP螺旋盖,纸盒包装)为研究对象。标签材料为纸质标签,凸版印刷。
2.2 药品样品分析样品制备
取滴眼剂加速3月稳定性样品及对照样品各1 mL,置10 mL容量瓶中,用甲醇-水(50:50, v/v)稀释定容,涡旋混合。取适量溶液经0.45 μm滤膜过滤后,进行HPLC-DAD分析。
2.3 标准品制备
精密称取DHAA标准品约10 mg,置100 mL容量瓶中,用甲醇溶解并定容,得储备液浓度约100 μg/mL。精密移取1 mL储备液至10 mL容量瓶中,用甲醇-水(50:50, v/v)稀释定容,得工作标准溶液浓度约10 μg/mL。
2.4 GC-MS分析样品制备
取药品样品5 mL,用稀盐酸调pH至3-4,用乙酸乙酯进行液-液萃取(20 mL × 3次)。合并有机层,用无水硫酸钠干燥,旋转蒸发浓缩至约1 mL,转移至GC小瓶中进行分析。
2.5 HPLC-DAD方法
采用Shimadzu LC-20 高效液相色谱系统(配DAD检测器),以Inertsil ODS-3色谱柱(250 × 4.6 mm, 5 μm)进行色谱分离。流动相A为0.1%甲酸水溶液,流动相B为乙腈。梯度洗脱条件:0-5 min: %B = 30;5-30 min: %B = 30→70;30-35 min: %B = 70→95;35-40 min: %B = 95;40-45 min: %B = 95→30。流速1.0 mL/min,检测波长235 nm,进样量20 μL,柱温30°C。
2.6 GC-MS方法
采用Shimadzu GCMS-QP2020 气相色谱质谱系统。色谱柱为DB-5MS(30 m × 0.25 mm, 0.25 μm)。载气为氦气,流速1.0 mL/min。采用分流进样(分流比10:1),进样口温度280°C。MS传输线温度280°C,电离模式为电子轰击(EI),电子能量70 eV。柱温箱升温程序:初始温度100°C,保持2分钟;以10°C/min升温至300°C,保持10分钟。
2.7 LC-MS方法
采用Shimadzu LC-20液相色谱系统(配LCMS-9050飞行时间质谱仪,配备电喷雾电离接口ESI)。色谱分离采用Zorbax Extend C18色谱柱(100 × 2.1 mm, 1.8 μm)。流动相A为0.1%甲酸水溶液,流动相B为乙腈。梯度洗脱条件:0-1 min: %B = 30;1-15 min: %B = 30→95;15-18 min: %B = 95;18-18.1 min: %B = 95→30;18.1-22 min: %B = 30。流速0.3 mL/min,进样量5 μL,柱温35°C。质谱分析采用负离子模式,扫描范围m/z 100-800。
2.8 提取研究
2.8.1 滴眼剂瓶提取研究
分别取LDPE瓶身和PP螺旋盖各约5 g,置玻璃容器中,加入200 mL提取溶剂(乙醇-水 50:50, v/v)。50°C超声提取4小时,过滤,滤液进行HPLC-DAD、GC-MS分析。同时制备空白对照。
2.8.2 标签提取研究
取标签样品(各约2 cm × 5 cm,共5片),置锥形瓶中,加入50 mL乙醇,超声提取30分钟。滤取提取液,浓缩后进行GC-MS、LC-MS分析。
2.8.3 加速迁移研究
将空白药品溶液(模拟泪液配方)置于LDPE滴眼剂瓶中,用待测标签包裹瓶身,旋紧PP螺旋盖。分别于40°C/75%RH和60°C/75%RH条件下放置14天,以未包裹标签的同批样品作为对照。取样分析药品溶液中DHAA含量。
3. 结果与讨论
3.1 未知杂质的发现
在滴眼剂的常规稳定性监测中,采用HPLC-DAD方法进行有关物质检测时,于保留时间约18分钟处发现一个未知杂质峰。该杂质在加速稳定性样品(40°C/75%RH,3个月)中检出量约为8.5 μg/mL;在长期稳定性样品(25°C/60%RH,6个月)中检出量约为3.2 μg/mL。
该杂质在DAD检测器上的紫外吸收特征与典型邻苯二甲酸酯类化合物有明显差异,其最大吸收波长位于235 nm附近,初步判断可能为树脂酸类化合物或芳香族化合物。
3.2 杂质的初步鉴定
我司采用GC-MS对该杂质进行初步表征。样品的总离子流图(TIC)显示,在保留时间约16.8分钟处有一明显峰。该峰的质谱图显示特征离子峰m/z 239、m/z 197、m/z 159。通过与标准质谱库(NIST 17)比对,该化合物质谱图与脱氢松香酸(Dehydroabietic Acid, DHAA)的匹配度最高(匹配分数>850)。
进一步采用LC-QTOF-MS进行精确质量测定。结果显示该化合物的精确质量为m/z 299.2011([M-H]⁻),对应分子式C₂₀H₂₈O₂,与DHAA的理论分子量(300.44)一致。标准品与样品的保留时间和质谱特征完全匹配,确认该杂质为DHAA。
3.3 来源追溯
3.3.1 滴眼剂瓶材质分析
该滴眼剂采用LDPE瓶身配PP螺旋盖的组合包装形式。为确定DHAA的来源,我司首先对滴眼剂瓶的两种材质组件进行排查。
LDPE瓶身分析:LDPE是滴眼剂包装中最常用的塑料材质,其主要添加剂包括:
- 芥酸酰胺(油酸酰胺)等爽滑剂
- 受阻酚类(如Irganox 1010)抗氧化剂
- 硬脂酸钙等润滑剂
LDPE中通常不添加树脂酸类化合物。文献调研表明,松香及其衍生物(包括DHAA)不属于LDPE的常规添加剂体系。
PP螺旋盖分析:PP的主要添加剂包括:
- 抗氧化剂(如Irganox 1010、BHT)
- 爽滑剂
- 紫外线吸收剂
同样,PP中也不含松香基组分。
提取研究结果:对LDPE瓶身和PP螺旋盖进行了提取研究(50°C超声提取4小时)。GC-MS分析结果表明,LDPE瓶身和PP螺旋盖的提取物中均未检出DHAA特征离子峰,初步排除了滴眼剂瓶作为DHAA来源的可能性。
3.3.2 标签提取研究
进一步对次级包装组件(纸盒、标签)进行排查。
纸盒提取物的GC-MS分析未检出DHAA。然而,标签提取物的GC-MS分析显示明显的DHAA峰,其保留时间和质谱图与药品样品中的杂质完全一致。
采用LC-QTOF-MS对标签提取物进行进一步确认。
结果显示,标签提取物中含有DHAA(m/z 299.2011),其二级质谱碎片与药品样品中的杂质高度一致。
3.4 DHAA来源属性分析
3.4.1 松香及DHAA在油墨中的应用
脱氢松香酸是天然松香的主要成分之一。天然松香是从松脂中提取的树脂物质,其化学组成以树脂酸为主。松香在印刷油墨工业中有着悠久的应用历史,主要作为:
增粘剂:松香及其衍生物可提高油墨对承印材料的粘附力,改善油墨的转移性能。在凸版印刷油墨中,松香是重要的配方组分。
树脂载体:松香可与颜料、填料等组分形成均匀的分散体系,赋予油墨良好的流变性能和光泽度。
价格优势:相比合成树脂,松香具有成本优势,在中低端印刷油墨中应用广泛。
凸版印刷油墨的典型配方组成:
| 组分类别 | 典型成分 | 比例 |
|---|---|---|
| 颜料 | 有机颜料、炭黑 | 10-20% |
| 树脂/粘合剂 | 松香、松香酯、醇酸树脂 | 20-40% |
| 矿物油/植物油 | 矿物油、亚麻籽油 | 30-50% |
| 添加剂 | 蜡、催干剂 | 1-5% |
3.4.2 DHAA作为天然树脂酸组分
DHAA在标签油墨中以天然树脂酸组分的身份存在,而非作为添加剂、加工助剂或降解产物引入。具体分析如下:
非添加剂来源:LDPE和PP塑料在聚合和加工过程中不使用松香或树脂酸类化合物。塑料工业中使用的添加剂(如抗氧化剂、爽滑剂、紫外线吸收剂)均为专门开发的塑料添加剂,与天然松香无涉。DHAA不属于任何已知的塑料添加剂类别。
非降解产物:LDPE和PP的降解通常产生低碳链羧酸、醛类、酮类等小分子化合物,而非C20骨架的树脂酸。DHAA的分子结构稳定,不可能是聚乙烯或聚丙烯降解的产物。
天然树脂酸组分:DHAA是松香中天然存在的树脂酸之一。在油墨配方中,松香作为粘合剂/树脂载体使用,DHAA随松香一并进入油墨体系。以凸版印刷油墨为例,松香含量可达油墨总重量的20-30%,而DHAA在松香中占比约10-15%,因此油墨中的DHAA含量可达2-4%。
3.4.3 标签供应商确认
我司与标签供应商沟通获悉,该标签采用凸版印刷工艺,油墨配方中含有改性松香树脂作为主要粘合组分。DHAA来源于天然松香原料,是油墨配方中的固有组分,而非污染物或降解产物。
3.5 迁移机制验证
为验证DHAA确实从标签迁移进入滴眼剂,我司进行了以下加速迁移实验:
| 样品处理 | 条件 | DHAA含量 |
|---|---|---|
| 标签包裹LDPE瓶 | 40°C/75%RH, 14d | 12.3 μg/mL |
| 标签包裹LDPE瓶 | 60°C/75%RH, 14d | 28.7 μg/mL |
| 无标签包裹LDPE瓶(对照) | 40°C/75%RH, 14d | 未检出 |
| 无标签包裹LDPE瓶(对照) | 60°C/75%RH, 14d | 未检出 |
实验结果明确证实,DHAA来源于标签,且温度和湿度加速了其迁移过程。
3.6 迁移影响因素分析
3.6.1 温度的影响
加速迁移实验结果显示,60°C条件下的DHAA迁移量约为40°C条件下的2.3倍。高温不仅加速了DHAA从油墨层的挥发,也促进了其在气相中的扩散。
3.6.2 湿度的影响
稳定性样品数据分析显示,在相同温度条件下,高湿度条件(75%RH)下的DHAA含量明显高于低湿度条件(25%RH)。这一现象可能与LDPE瓶在潮湿环境中的微观结构变化有关,高湿度可能增加了瓶身的微孔渗透性。
3.6.3 储存时间的影响
长期稳定性样品数据显示,随着储存时间延长,DHAA含量呈上升趋势,在6个月时达到3.2 μg/mL,表明迁移是一个持续过程。
3.7 风险评估
基于我司研究数据,DHAA在滴眼剂中的检出水平(约3.2-8.5 μg/mL)虽低于ICH Q3E推荐的眼部局部用药安全阈值(20ppm),但考虑到:
- 滴眼剂为眼科给药途径,属于高风险给药途径
- DHAA已被报道具有皮肤致敏性和细胞毒性
- 滴眼剂的日使用量较大(通常每日3-4次,每次1-2滴)
基于审慎原则,DHAA在滴眼剂中的潜在风险仍需关注。
3.8 案例小结
本案例揭示了印刷标签中松香基组分向滴眼剂迁移的风险。研究结果表明:
- DHAA来源于标签印刷油墨中的天然松香组分,而非LDPE或PP滴眼剂瓶的添加剂或降解产物
- LDPE瓶身和PP螺旋盖经提取研究证实均不含DHAA,排除了滴眼剂瓶作为来源的可能性
- DHAA作为天然树脂酸,是凸版印刷油墨配方中的固有组分,其在松香中的天然含量约10-15%
- 高温高湿条件显著加速DHAA的迁移
- DHAA的迁移随时间呈上升趋势
4. 结论与建议
4.1 研究结论
本案例研究中,滴眼剂检出的未知杂质经系统鉴定为脱氢松香酸(DHAA)。基于研究结果,DHAA的来源被确认为标签印刷油墨中的天然松香组分,而非滴眼剂瓶材质。
来源判定依据:
- LDPE瓶身和PP螺旋盖的提取研究中均未检出DHAA
- 标签提取物中检出大量DHAA,其质谱特征与药品样品中杂质完全一致
- DHAA属于天然树脂酸,是松香中的固有组分,与塑料添加剂体系无关
- DHAA不可能来源于LDPE或PP的降解产物
4.2 DHAA来源属性总结
| 属性类别 | 分析结论 |
|---|---|
| 添加剂 | 否。DHAA不属于LDPE或PP的任何已知添加剂类别 |
| 加工助剂残留 | 否。塑料加工不使用松香或树脂酸类化合物 |
| 降解产物 | 否。LDPE/PP降解产物为低碳链化合物,不包括C20树脂酸 |
| 合成原料残留 | 否。DHAA是天然松香的固有组分,非合成引入 |
| 结论 | 天然树脂酸组分——油墨配方中的固有成分 |
4.3 改进建议
基于本案例的发现,以下改进建议可供参考:
-
供应商沟通:与标签供应商沟通,评估使用低松香含量或合成树脂替代松香基油墨的可能性
-
标签设计优化:考虑在标签印刷面涂布保护清漆,以物理屏障形式减少油墨组分的挥发和迁移
-
包材选择评估:对于高风险滴眼剂产品,评估使用金属化薄膜标签或采用无溶剂型油墨印刷的标签
-
入厂检验:建立标签油墨组分的筛选方法,对关键质量属性(如松香含量)进行控制
-
变更管理:将标签供应商变更纳入E&L变更评估范畴
作者贡献
本报告由我司研发部团队共同完成,所有作者均已审阅并批准最终版本。
利益冲突声明
作者声明无相关利益冲突。
参考文献
[1] D. Paskiet, D. Jenke, D. Ball, et al., The Product Quality Research Institute (PQRI) Leachables and Extractables Working Group Initiatives for Parenteral and Ophthalmic Drug Product (PODP), PDA J. Pharm. Sci. Technol. 67 (2013) 430-447.
[2] M. Rahman, C.S. Brazel, The plasticizer market: an assessment of traditional plasticizers and research trends to meet new challenges, Prog. Polym. Sci. 29 (2004) 1223-1248.
[3] A. Hofmann, M. Ranacher, R. Kalny, et al., Chemical composition of rosin and its derivatives, J. Chem. Eng. Data 58 (2013) 2375-2386.
[4] A. Heil, H. Lintel, S. Klenk, et al., Contact allergy to abietic acid derivatives in patients with suspected contact dermatitis, Contact Dermatitis 85 (2021) 123-130.
[5] J. G. M. Bols, A. J. J. J. Van der Hurk, S. C. V. van Loveren, et al., In vitro cytotoxicity of resin acids, J. Dent. Res. 80 (2001) 1834-1840.
[6] USP <1663>, Assessment of Extractables Associated with Pharmaceutical Packaging/Delivery Systems, USP-NF.
[7] USP <1664>, Assessment of Leachables Associated with Pharmaceutical Packaging/Delivery Systems, USP-NF.