强调了密封件的选择和确认研究的重要性。介绍了药品与密封件相容性研究的重要性和试验方法,包括密封件组分进行提取试验和模拟提取试验,选择合适的提取介质和检测方法,以及可提取物进行风险评估和预测可能的浸出物。提出了浸出物研究和试验结果安全性评估的方法。
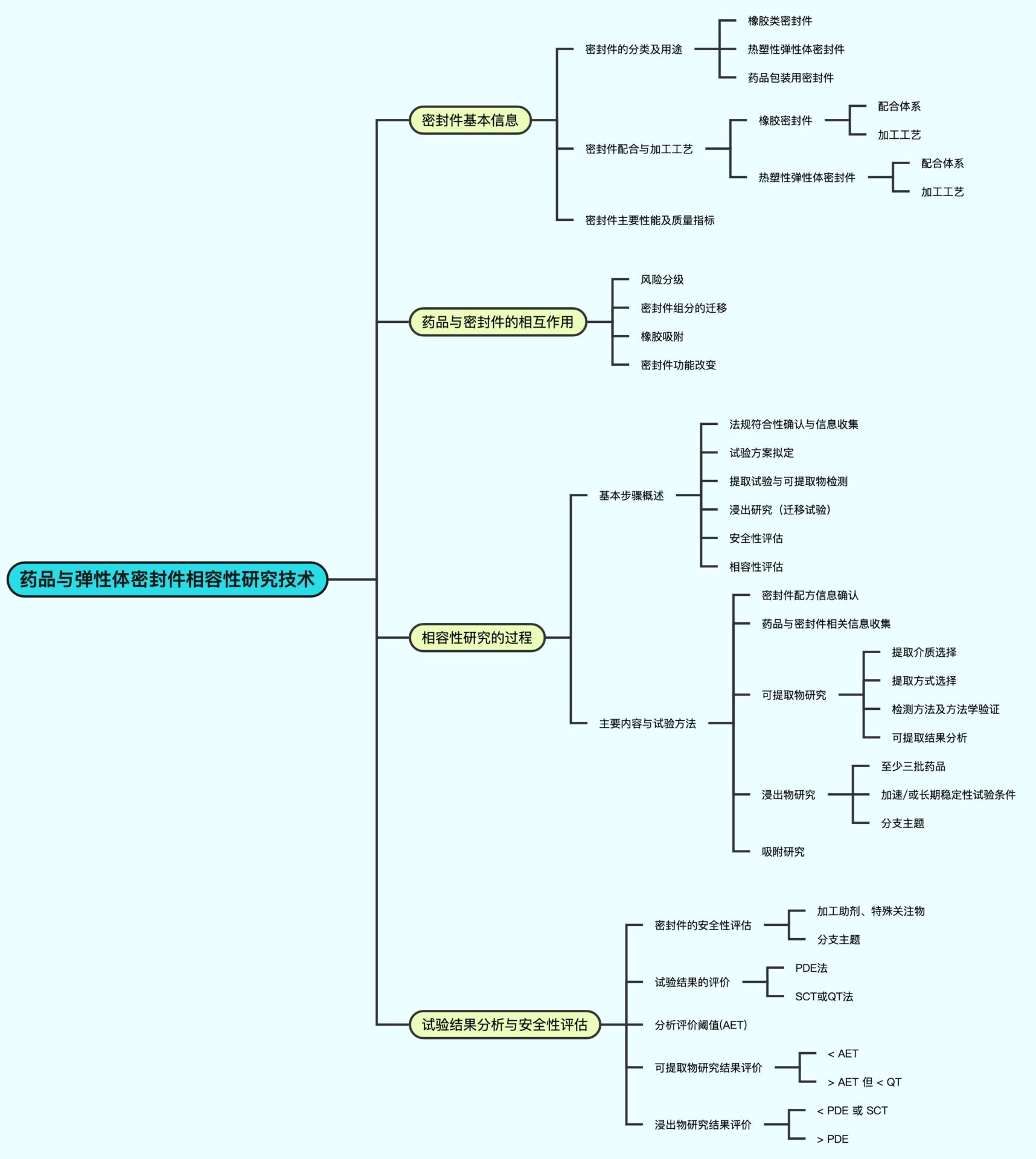
相容性研究的步骤
- 收集相关信息:收集与密封件相关的配方信息、加工助剂信息、清洗剂和清洗方式、硅油、涂层材料、灭菌等信息,同时收集药物制剂的处方、工艺、给药途径、给药频率及给药剂量等信息。
- 确认法规符合性和质量标准符合性:确认密封件组分的法规符合性以及密封件产品的质量标准符合性,并收集进行相容性试验所需要的基本信息。
- 制定相容性研究的试验方案:根据密封件及药品的特点,确定试验样品的批次及数量,制定提取试验样品的制备方法,开发针对相应可提取物的检测方法等。
- 进行相容性研究试验:根据试验方案,进行密封件的提取试验和/或模拟提取试验,对可提取物进行检测方法的研究,进行风险评估并预测可能潜在的浸出物。
- 试验结果分析与安全性评估:对试验结果进行分析,根据浸出物的含量和性质进行安全性评估,比较浸出物的水平与安全性阈值的关系,评估可能的安全性风险。
- 作出密封件是否与药品具有相容性的结论。
可提取物研究
对密封件材料进行提取试验和/或包装容器系统的模拟提取试验,研究材料中可提取的无机或有机物,包括基体材料成分、加工助剂、配方添加物的降解物以及其之间的反应产物等。
浸出物研究
通过浸出物研究,了解药品或模拟药品与密封件实际接触时提取得到的无机或有机可提取物。需要考虑药品的制备工艺条件、药品与密封件接触的实际情况。
应至少采用三批药品进行浸出物研究,可参考加速及长期稳定性试验的考察时间点设置。
检测方法及方法学验证
根据可提取物的性质和测试目的选择适宜的分析方法,并进行方法学验证,确保方法的准确度、灵敏度和稳定性。
对浸出物测试方法进行全面的方法学验证,包括准确度(回收率)、精密度(重复性、中间精密度)、专属性、检测限、定量限,线性和范围等。
试验结果评价和安全性评估
对超过安全性评估阈值的可提取物和浸出物进行鉴定和安全性评估,判断其对人体是否有害。
- 对于不超过 AET 的可提取物,可认为该可提取物导致的安全性风险小,在后续的浸出物研究试验中可省略对该可提取物的研究。
- 对于高于 AET 的可提取物,需进行鉴别或结构确认以及半定量分析,进行初步毒理学评估以判断该物质是否对人体有害。
- 如果浸出物含量低于人每日允许暴露量(PDE)或 SCT时,可认为浸出物的水平对人体产生的风险是可以接受的。
- 如果浸出物的含量高于 PDE,则认为浸出物的水平所产生的风险是不可以接受的.