针对与药品直接接触的组件和材料,各监管部门均要求应评估可提取物和浸出物(E&L),以确定浸出物污染药品的风险。与药品长期储存接触的容器封闭系统的风险高于短时间接触产品的工艺设备。但是,工艺设备的浸出物风险评估也不能忽视。
一次性使用系统(SUS) 的聚合物材料可能向制造过程引入一系列化合物,如单体、稳定剂、润滑剂、滑石粉、颜料和抗氧化剂等。为确保患者安全,必须系统评估和控制系统中任何提取物和浸出物带来的风险
制药工艺中使用的SUS种类繁多,开展浸出研究可能耗时昂贵,因此优化浸出评估或测试对提高生产效率、降低成本非常重要。如图1所示,SUS包括生物反应器、混合袋、过滤器、管道、色谱柱、储液袋等。
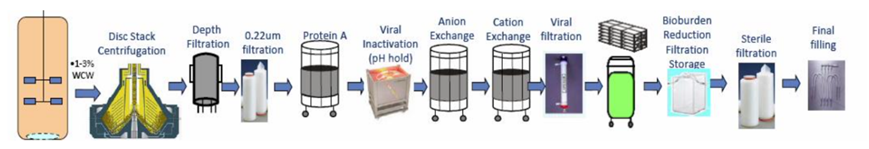 图1 生物制药工艺一次性组件系统
图1 生物制药工艺一次性组件系统
浸出物研究在基于提取试验和风险评估的基础上执行,相关的指南包括BioPhorum发布的标准化的可提取物方案、美国药典(USP)通用章节<665>和<166>、NMPA颁布的《化学药品注射剂生产所用的塑料组件系统相容性研究技术指南(试行)》,具体介绍详见文章“生产组件E&L系列 国内外提取研究指南介绍”、“ 生产组件E&L系列 风险评估”。通常制药企业可以获得一次性使用组件供应商提供的提取物数据,根据监管要求,制药企业有责任根据其特定工艺评估这些提取物数据,并在需要时生成浸出物数据,以确保安全合规的产品。
1|可提取物&浸出物
可提取物在相对于实际工艺条件下夸张的实验室条件下,从一次性使用系统提取的化合物
▼ 包括添加剂、低聚物、单体、添加剂和聚合物中的降解或反应产物、杂质等
▼ 选择不同极性的溶剂进试验
▼ 通常是供应商责任:提供可提取物信息过程设备相关渗出物(PERLs)
▼ 在模拟最坏工艺过程条件下从一次性使用系统浸提的化合物
▼ PERLs是可提取物的子集
▼ 最终产品中来自SUS使用的化合物
▼ 渗出物存在于药品中,被患者摄入风险
▼ 是制药企业的责任
2|如何利用可提取物数据
如何利用提取物数据和对制造工艺进行评估,是行业关注的焦点,目前尚无统一标准。但是如果提取物数据能够合理预测潜在的浸出物,那么这些数据将非常有价值。提取物数据可用于:
▼ 进行毒性评估
▼ 设计浸出物研究
▼ 提供免除浸出物研究的理由
要点1 风险评估
首先根据组件在工艺中的使用位置和条件进行风险评级。如果材料不是聚合物或聚合物材料不与工艺液体接触,则此类组件无需进一步评估,可以从风险评估中排除。对于所有与工艺液体接触的聚合物组件进行下一步风险评级,分为低风险、中风险和高风险。考虑的评估因素包括温度、接触时间、工艺液体性质、材料性质等影响浸出倾向的因素。在根据风险级别决定是否进行浸出研究时,应考虑制造操作的某些方面。
考虑的风险缓解因素包括:
(1)工艺步骤对浸出物的稀释或清除,某些工艺步骤将在很大程度上减少浸出物,例如:
▼ 在上游工艺中,从生物反应器中浸出的物质会在收获期间被除去
▼ 下游纯化过程中,膜过滤器的表面具有特异性清除能力
▼ 层析树脂或膜吸附剂具有特异性清除能力
▼ 超滤或洗滤UF/DF能有效去除小分子,研究表明,小分子浓度从负荷到最终滤液可减少100至10000倍
(2)临床应用
▼ 低风险剂型(如固体、液体口服制剂或局部剂型),则风险降级。
▼ 如果临床使用的持续时间<7 天,则风险降级。
▼ 如果每日临床使用剂量<10 mL,则风险降级。
要点2 确定后续测试
根据评风险级结果确定后续测试低风险组件
低风险组件
▼ 符合相关药典测试(如生物兼容性测试)要求中、高风险组件
中、高风险组件
▼ 组件除了药典测试要求之外,还需要具有支持性的提取物数据
▼ 对应用这些数据的详细论证,将研究条件与实际工艺条件进行比较
▼ 如不开展浸出试验,应提供科学解释
▼ 据来自提取物数据的潜在浸出物的最大剂量来确定毒性
▼ 如果潜在浸出物的存在风险,则可能需要进行浸出物测试和评估
▼ 如果潜在浸出物可能影响产品质量,则可能需要进行研究来评估对产品质量(包括有效性)的影响。
要点3 提取数据的可靠性
应审查提取试验设计的合理性,确认分析技术的可靠性和完整性。通常提取报告应至少包括以下内容:
▼ 参考指南
▼ 测试样品详细信息
▼ 实际工艺条件
▼ 测试项目概述
▼ 组件/样品处理方式
▼ 提取条件(温度、时间、提取方式、提取比例)
▼ 分析方法
▼ 报告限值
▼ 按各个分析方法全面列出可提取物
▼ 计算方式
▼ 可提取物汇总表毒理学评估结果
3|提取数据外推步骤
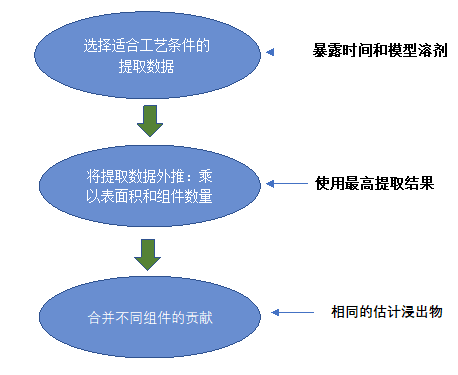
在大多数一次性使用系统(SUS)中,只有少量工艺相关的潜在浸出物(PERL)会成为实际存在于最终制剂中的浸出物,且通常以非常低的浓度存在。提取结果可用于预测药品中浸出物的范围和最大浓度,通过详细分析提取物谱,可以外推浸出物。提取物数据如何用于估计产品和患者暴露?可以采取以下步骤:
▼ 选择适合的提取数据,获得组件/材料每单位面积的可提取物水平。
▼ 结合实际工艺条件,计算工艺中可提取物的累积水平,代表潜在浸出物。
▼ 对结果进行安全评估,确定工艺生成的潜在浸出物是否存在安全风险。
 ## 4|如何获得不同尺寸组件的提取物数据?
## 4|如何获得不同尺寸组件的提取物数据?
由于一次性使用系统(SUS)种类繁多,不可能对市场上所有设备进行测试,可以根据不同产品系列的数据进行结果扩展。
通常采用两种方法:
▼ 对于短接触时间组件,可以根据组件接触表面积缩放提取物结果。基于扩散机制,提取物或浸出物的量与暴露表面积成正比。
注意:提取物数据获得的缩放结果仅对可获得的时间点有效。
▼ 对于长接触时间组件,可以在SUS材料与接触溶液之间达到平衡后,根据分配系数计算缩放结果。
类似于容器密闭系统(CCS),在产品保质期结束时,浸出物可能会达到或接近平衡浓度。
4|计算案例
- 计算过程
某组件提取研究表明,发现12种提取物化合物,报告水平≧10ug,最高的化合物水平为241.5mg(抗氧剂降解物2,4-二叔丁基苯酚)。
假设:工艺规模为1批次,生产的产品为10Kg,临床使用途径为静脉注射,剂量为10mg/天。
暴露量=提取物/生产规模 × 剂量最高
暴露量= 241.5mg/10 kg× 10mg/天 = 0.24ug/天。
- 毒理学评估
在经典的毒理学评估中,可以根据提取物数据估计潜在的患者日暴露量,并与毒理学关注阈值(TTC)或允许的日暴露量(PDE)进行比较,以确定安全边际。TTC值可在多份文献中找到,包括ICH M7指南。
表 I CH M7单个杂质的可耐受每日摄入量
 对于治疗期大于10年至终身的药品,TTC值为1.5μg/天,低于此限值的日摄入量导致癌症风险小于十万分之一,其风险可忽略不计,因此TTC可作为大多数药品可接受限值的默认值。
对于治疗期大于10年至终身的药品,TTC值为1.5μg/天,低于此限值的日摄入量导致癌症风险小于十万分之一,其风险可忽略不计,因此TTC可作为大多数药品可接受限值的默认值。
如果采用保守计算的提取物最大日暴露量低于TTC限值,则可以推断检测到的其他较低水平提取物的日暴露量也低于该限值。因此,安全风险是可以接受的。
- PDE值计算
PDE=NO(A)EL×体重调整/[F1×F2×F3×F4×F5×F6]
以抗氧剂降解物2,4-二叔丁基苯酚为例:
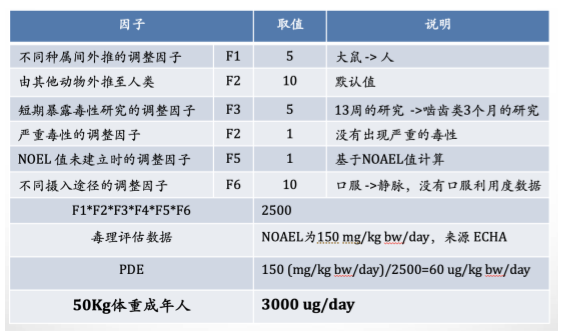 安全边际MOS=PDE/最高暴露量=3000(ug/天)/0.24(ug/天)=12500 >1
安全边际MOS=PDE/最高暴露量=3000(ug/天)/0.24(ug/天)=12500 >1
安全边际大于1, 可提取物的安全风险是可以接受的。
| 总结 |
尽管目前还没有统一的指导性文件,但是监管要求对直接接触药物生产工艺流的制造组件进行风险评估。一旦获得科学合理的提取物数据,可以根据生产批次大小和给药方案针对药品进行安全评估。
E&L风险分析是一个复杂过程,现有的可提取物数据可以帮助SUS制造商加速产品资格认定和风险评估,推动制药企业工艺优化和使用效率提高。
一次性使用组件设计日趋复杂,全球性指南和行业共识快速变化。在此背景下,要求合同实验室快速响应,设计符合规范的实验方案,采用多种分析技术检测和定量不同类型提取物,尤其是对未知成分进行鉴定,提供可靠的数据,这对确保合规和药品安全具有重要意义。
如您面临数据利用不足,难以说服监管机构的情况,伯朗氏实验室可提供提取数据评估和利用方案,帮助企业降低费用支出,提高生产效率!
参考文献
BioPhorum, BioPhorum Best Practices Guide for Extractables Testing of Polymeric Single-Use Components Used in Biopharmaceutical Manufacturing (BioPhorum, 2020).
-
USP, General Chapter <665>, “Plastic Components and Systems Used to Manufacture Pharmaceutical Drug Products and Biopharmaceutical Drug Substances and Products,” USP–NF, (Rockville, MD, 2022).
-
USP, General Chapter <1665>, “Characterization and Qualification of Plastic Components and Systems Used to Manufacture Pharmaceutical Drug Products and Biopharmaceutical Drug Substances and Products,” USP–NF (Rockville, MD, 2022).
-
国家药监局药审中心(通告(2020年第33号):化学药品注射剂生产所用的塑料组件系统相容性研究技术指南(试行)-2020年10月.
-
Hauk A, et al. On the “Fate of Leachables” in Biopharmaceutical Up-Stream and Down-Stream Processes. Single-Use Technologies II: Bridging Polymer Science to Biotechnology Applications. Proceedings of Biopoly II, Tomar, Portugal, 7–10 May 2017.









