本文比较了固体冻干制剂与液体制剂中浸出物的差异,并探讨了该差异产生的机制。
在固体制剂中检出更高水平的浸出物,这与药品配方配方的非水性特征和化合物的疏水性相关。深入理解固体药品与其包装材料之间的相互作用机制及影响因素,这对于确保包装不会对药品的安全性和有效性产生不利影响至关重要,也是实验室进一步研究的方向。
内容开始之前,首先我们提出两个问题:
Q1:冻干制剂中浸出物的可能性必然低于低于液体制剂吗?
Q2:冻干制剂与包装材料之间发生相互作用的可能性可以忽略吗?
从直观判断和参考《化学品与橡胶密封件相容性研究技术指南(试行)》来看,注射液与包装发生相互作用的可能性高于粉末。但是,如果Q1的答案为“是”,总会有一点点疑问。对于低风险的冻干粉制剂,Q2的答案似乎也不能忽略,为什么呢?
接下来,我们就一起来从冻干制剂的理化性质、冻干制剂中浸出物存在的现象和机理,结合试验结果来探讨以上的问题。
1. 背景介绍
冻干(也称为冷冻干燥)是一种利用降低的温度和压力来代替加热来去除物质中水分的过程,这种固体制剂通常用于在溶液中化学或生物不稳定的药物产品,是许多生物制药类产品所遇到的情况。因此,随着生物制药需求的增加,市场上冻干制剂的数量也在增加。
与任何药品一样,有必要确定用于储存冻干制剂的包装系统不会引入可能对其安全性和/或疗效产生负面影响的杂质。这通常是通过药品和包装材料相容性研究,即提取研究和浸出研究来实现。
尽管冻干药物制剂的流行率越来越高,目前多数研究主要集中在液体药物制剂,物质从包装系统浸出至溶液中是常见和容易理解的,冻干产品或其他固体介质与包装系统的相互作用尚未得到彻底探索。
对于固体的冻干药物制剂,可能会倾向于简单地得出结论,认为它们无法从接触的包装系统中溶出材料中添加剂、聚合单体及其降解物等,或者此类浸出物产生的可能性很低。毕竟,一个固体如何能像溶液一样从包装材料中溶解出物质?这种假设在相容性研究技术指导原则中药物风险矩阵中是显而易见的,该矩阵将粉末与包装发生相互作用的可能性分级为“低可能性”。
表 1 不同给药途径药品的风险分级及其与包装组件发生相互作用的可能
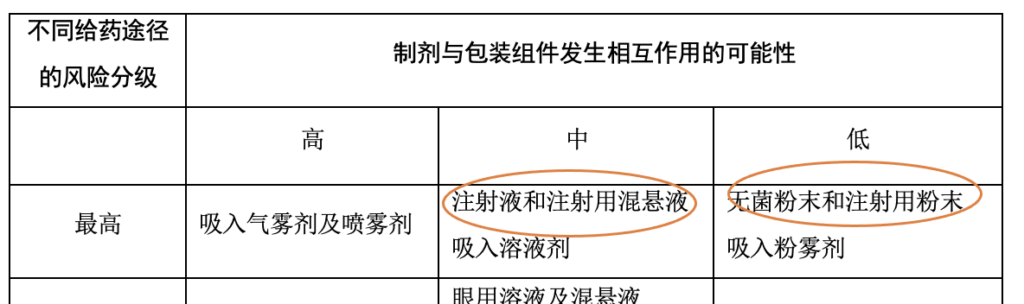
然而,真实的情况恰恰相反,越来越多的试验结果表明,在固体冻干药物制剂中检出来源于内包材的浸出物,甚至对于某些化合物,在冻干药物制剂中有较高的溶出风险,即“与存储在相同包装中的液体制剂相比,源于丁基橡胶塞的某些物质对固体冻干药物制剂有更高的亲和力”。
2. 冻干制剂的提取研究
就包装系统中浸出物的速率和/或水平而言,目前的研究还不能完全明确固体冻干制剂与液体制剂(或者固体与液体介质)之间存在哪些差异(如果有的话)。因此,尽管冻干药物是固体,在进行提取物研究时使用溶剂来模拟药品是可行的,也有助于更好地进行材料化学表征。
提取研究的一个目标是使用更强力的提取溶剂和测试条件来进行材料化学表征,在这种情况下,可通过回流、湿热灭菌、提高有机溶剂比例等方式来提取冻干制剂的包装组件。
另一个目标可以是预估产品实际的浸出物,进行定性/定量。在这种情况下,需要依据辅料或API的浸出能力特性来选择各种水/有机溶剂混合物,在合适的实验室条件下来模拟产品储存和使用期间的实际接触,同时实验室应掌握这些介质(而不是药物基质)的分析兼容性。
在选择模拟溶剂时必须非常谨慎,因为固体制剂和液体制剂之间可能发生不同的相互作用。例如,考虑到可浸出物的疏水性,使用高水性溶剂将不足以模拟冻干药物。有研究表明需要用到50/50醇/水的溶液来模拟冻干药物产品的提取能力。
3. 存储过程中的浸出
为确定和比较液体制剂和固体制剂中的浸出物,试验选择了3种冻干制剂和3种液体制剂,以中硼硅玻璃注射剂瓶和卤化丁基橡胶塞作为包装系统。
通过前期的提取研究,已确定丁基橡胶塞中主要的可提取物为常见的抗氧剂BHT(CAS ),以及来源于材料的系列低聚物(C13H21、C21H40和相应的卤代物)。以这些化合物作为目标物的原因是基于它们作为挥发性浸出物,在丁基橡胶材料中普遍存在。
虽然没有市售的低聚物标准物质,但这些化合物已在科学文献中进行了表征,感兴趣的读者可以参照“”,该文介绍了低聚物的质谱图、化学结构和聚合过程中的详细信息,伯朗氏实验室通过制备分离,已将其加入到自有的气相色谱/质谱的光谱库中。
表2 试验药品信息
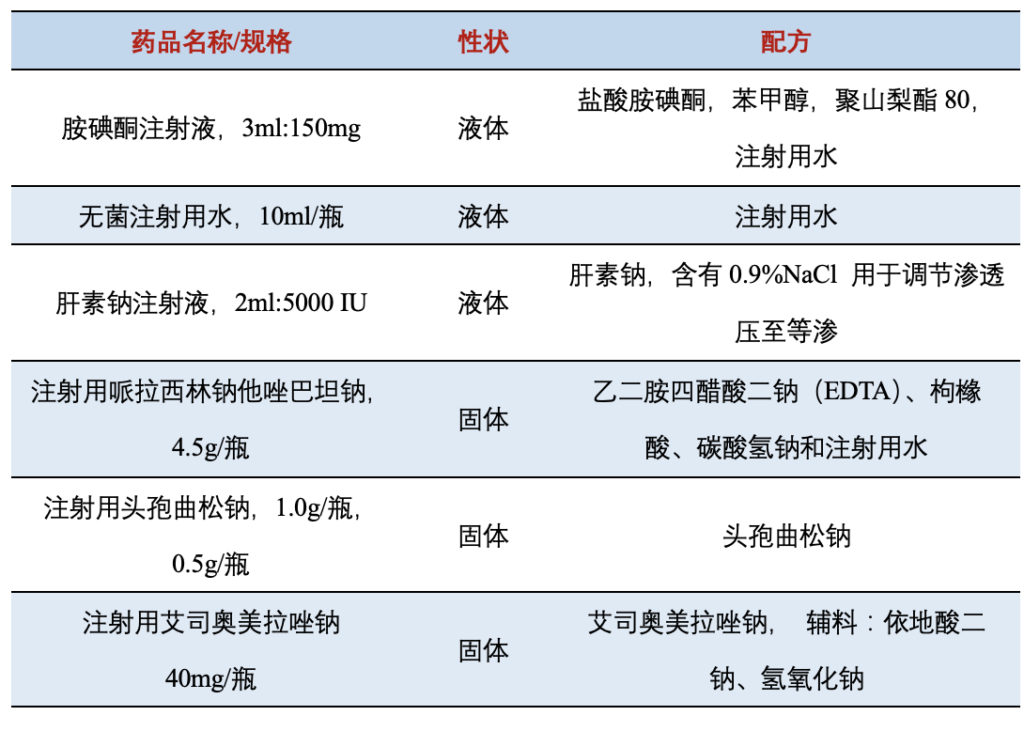
试验条件
每种药物产品在60℃下倒置培养60天。之所选择这种接触温度和持续时间,是根据美国测试与材料协会(ASTM)关于医疗设备加速老化的指南中描述的Q10温度系数(依据阿伦尼乌斯公式Arrhenius equation),60℃下60天相当于在环境温度下的储存时间约为2年。
分析方法
采用基于单离子监测气相色谱/质谱(SIM-GC/MS)的方法对目标物进行分析。选择GC作为色谱系统的原因是因为它适用于分析样品中相对挥发性的物质,质谱仪作为检测器可满足研究对定性的需求,即能够明确识别在各种样品中发现的目标物质,并将其与其他无关的物质区分开来。
由于水性液体和复溶的冻干药物溶液与GC/MS分析方法不兼容,采用了SPE方法进行预处理,通过加标回收率测试验证预处理过程。
取抗氧剂BHT标准物质制备50ng/mL至100μg /mL范围的系列标准溶液,以校准曲线进行定量。低聚物以苯乙酮-D8作为替代标准进行定量。
试验结果
固体制剂浸出物浓度以μg/g为单位,液体制剂浸出物浓度以μg/ml为单位。
以低聚物C13H21的结果为例,不同药品中的浸出量见下图。
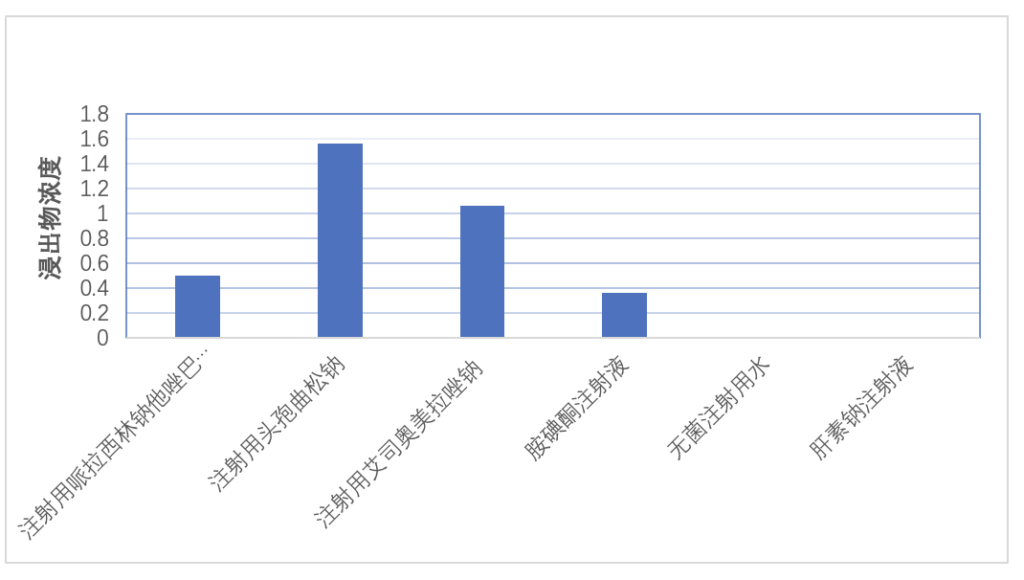
试验结果表明,当目标化合物存在于橡胶塞中时,在冻干制剂中都可检测到这些化合物,而液体制剂只在胺碘酮注射液中检测到这些化合物,可见冻干制剂对这些物质的亲和力超过液体制剂。
原因在于胺碘酮注射液中存在的增溶剂(聚山梨酸酯80),促进了物质的溶出。而无菌注射用水和肝素钠注射液中不含增溶剂,溶出物非常微量,不能被检出。
特别要指出的是,这些化合物都具有疏水性,因此液体制剂中水的存在增加了介质极性,显著降低了对该类化合物的溶解性或亲和力,最终减少了它们作为浸出物而存在的可能性。相反,冻干制剂不含水,这降低了药品的极性,因此增加了对这些化合物的亲和力。
另外,目标化合物都是相对低分子量的半挥发型物质,最终通过气体/蒸汽相迁移进入产品中,一定程度的挥发性将有助于它们从橡胶塞中扩散到固体药物中,即使通常认为固体相对于液体相而言被视为“静态”介质。
而具极性的化合物,在水基性药品中更容易被溶解,更有可能作为浸出物在液体制剂中出现,这些化合物未含在本次讨论范畴。
无论药物基质性质的变化如何,可以推断,给定固态或液态制剂中的特定浸出物的种类及其浓度水平取决于瓶塞的组成。就浸出物的定性方面而言,如果某个化合物不在橡胶塞中存在,那么它就不会以浸出物的形式存在。就浸出物的定量方面而言,如果橡胶塞中存在更高浓度水平的物质,那么在橡胶塞中的储备池耗尽或平衡的情况下,将观察到更高水平的浸出物。
3. 在临床使用时发生了什么
先前讨论的浸出物数据基于冻干制剂在包装系统中储存后的溶出量。然而,在实际临床使用过程中,这些药物通常不是以冻干形式直接给药给患者的,因此,在临床使用时存在冻干制剂中浸出物不一定全部暴露于患者的可能性。
例如,通常先采用水性介质中复溶冻干药物,然后通过注射器、袋、泵和/或输液器储存和/或给药。那么,这些前述的疏水性化合物是否在整个过程中持续保留在药物溶液中?或者是否这些化合物会通过某种机制消失,例如沉淀或与储存/给药系统结合?
有研究报道,复溶的冻干制剂与给药系统在接触一段时间后,来自包装材料的浸出物浓度水平下降,甚至有的浸出物浓度会降低到无法检测。
这项研究的结果也表明,这种减少的幅度是时间、温度和每种浸出物性质的函数,对于这些变量的某些组合,患者所暴露的浸出物并没有消除,甚至没有减少。因此,必须进一步考虑这些变量对每种可浸出物的影响,以充分了解这种相互作用的范围及其对患者暴露的最终影响。
后续我们还将继续讨论并评估冻干制剂中浸出物在整个储存/给药过程中的浓度变化情况。评估的变量包括与给药系统的接触持续时间和接触温度,以及给药装置的材质(例如PVC与非PVC材料)。
4. 结论
至此,对于本文开始的问题,我们可以做出总结。
Q1:冻干制剂中浸出物的可能性必然低于低于液体制剂吗?
概括而言, 在普遍的情况下答案为是的。但在具体情况下,当其他所有变量相同时,与液体制剂相比,冻干制剂可能含有更多、浓度更高的某些浸出物。考虑到介质的不同性质和目标浸出物的理化性质,这种差异是合理的,值得注意。
Q2:冻干制剂与包装材料之间发生相互作用的可能性可以忽略吗?
作为Q1的延伸,这个问题应该比较清楚了,不能忽略。
当前冻干制剂与包装材料之间的相互作用研究支持了这样一个结论,即与液体药物配方相比,来自橡胶塞的某些常见化合物对冻干药物配方表现出更高的亲和力。
然而,重要的是要理解固体药品配方的化学组成如何影响浸出物,以及其他因素(例如表面性质的变化)是否与溶出程度相关等机理,对于这些不确定性因素,目前在整个制药行业还未达到统一认识。
随着市场不断增加的冻干药物产品数量,重要的是要理解这类产品与其包装系统的相互作用机制,以确保包装材料不会对其安全性和功效产生负面影响。
参考文献
- 化学药品与弹性体密封件相容性研究技术指导原则(试行)
- Williams NA. The lyophilization of pharmaceuticals: a literature review. PDA J Pharm Sci Tech. 1984;38(2):48-59.
- Zdravkovic S. Comparison of a lyophilized drug product to other solid and liquid media for the extraction of elastomeric oligomers from a butyl rubber stopper. PDA J Pharm Sci Tech. 2017;71(6):488-501.
- Zdravkovic SA. Comparison of the solubilization properties of polysorbate and isopropanol/water solvent systems for organic compounds extracted from three pharmaceutical packaging configurations. Eur J Pharm Sci. 2016;93:475- 483.
- Jenke DR. Evaluation of model solvent systems for assessing the accumulation of container extractables in drug formulations. Int J Pharm. 2001;224:51-60.
感谢阅读🙏,求关注公众号🤭,网址和联系方式见下,随时恭候🌹

伯朗氏实验室: https://www.brunslab.com
联系电话:18816792607









