1. 什么是液相色谱
液相色谱(Liquid Chromatography,LC)是一种物理化学分离技术,它的核心任务是:把混合物拆成单一组分。
这个过程发生在一个由两相组成的系统中:
- 固定相(Stationary Phase):静止不动的一相,通常是固体吸附剂(如硅胶)或涂覆在固体载体上的液体。
- 流动相(Mobile Phase):不断流动的一相,通常是液体溶剂或溶剂混合物。
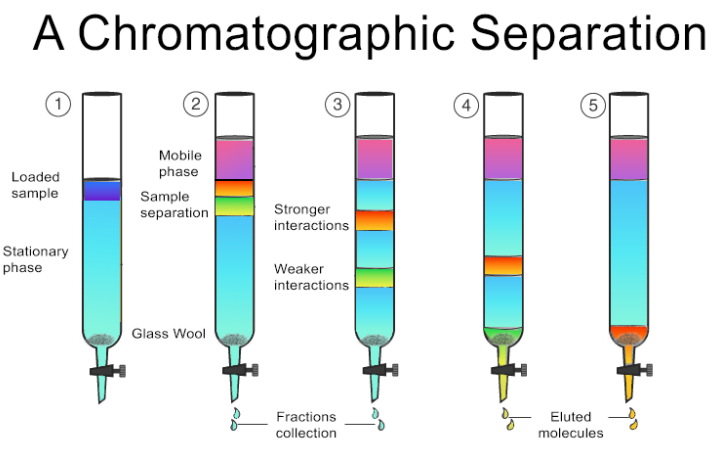
2. 分离是如何发生的
2.1 核心机制:可逆平衡
Sorbtech手册指出,色谱分离依赖于可逆平衡机制。当流动相携带样品通过固定相时,样品中的各个组分会在两相之间不断分配:
吸附 解吸
┌──────────┐ ┌──────────┐
│ 固定相 │ ←──────→ │ 流动相 │
│ (保留) │ │ (洗脱) │
└──────────┘ └──────────┘
↑ ↑
└──────── 平衡 ────────┘2.2 为什么不同分子会分开
每个分子与固定相的"亲和力"不同,这种亲和力由以下因素决定:
| 因素 | 说明 |
|---|---|
| 极性 | 极性分子与极性固定相(如硅胶)亲和力强 |
| 分子结构 | 官能团类型影响吸附能力 |
| 分子大小 | 大分子可能无法进入孔道 |
| 电荷 | 离子型分子在离子交换色谱中受电荷控制 |
2.3 保留与不保留物质
这是一个关键概念:
- 保留物质(Retained):与固定相有相互作用,在柱中停留时间较长
- 不保留物质(Unretained):不与固定相作用,随流动相前沿直接通过
实践提示:在HPLC中,不保留物质的保留时间(t₀)代表死时间—这是计算所有其他组分保留参数的基础。
3. 色谱图解读
3.1 一张图看懂色谱图
当分离后的组分依次流出检测器,检测器信号对时间作图,就得到色谱图:
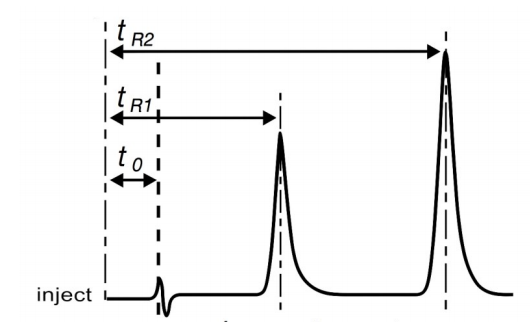
3.2 关键参数定义
| 术语 | 符号 | 定义 |
|---|---|---|
| 死时间 | t₀ | 不保留物质通过色谱柱的时间 |
| 保留时间 | t_R | 组分从进样到峰顶的时间 |
| 调整保留时间 | t_R’ | t_R – t₀,实际与固定相相互作用的时间 |
| 峰宽 | W | 峰基线宽度,反映柱效 |
| 保留因子 | k’ | 衡量保留程度的无量纲值 |
3.3 分辨率:分离的核心指标
分辨率(Rs) 衡量两个峰分离的程度:
Rs = 1:峰尖距离等于4σ,两个峰勉强分开
- Rs = 1.5:基线分离,这是我们的目标!
- Rs = 0:两个峰完全重叠
实践标准:只有达到 Rs ≥ 1.5 才能认为两组分真正分离。
4. 色谱模式
液相色谱有多种分离模式,选择哪种取决于样品性质:
4.1 正相色谱(Normal Phase)
固定相:极性(硅胶、氧化铝)
流动相:非极性到中等极性(正己烷→乙酸乙酯)
适用:非极性到中等极性有机化合物
原理:极性组分在固定相上保留更强
4.2 反相色谱(Reversed Phase)
固定相:非极性(C18、C8键合硅胶)
流动相:极性(水/甲醇、乙腈)
适用:大多数有机化合物、药物、蛋白质
原理:非极性组分在固定相上保留更强
⚠️ 这是目前最常用的HPLC模式!
4.3 其他模式
| 模式 | 固定相 | 原理 | 典型应用 |
|---|---|---|---|
| 离子交换 | 带电荷树脂 | 电荷吸引 | 氨基酸、蛋白质、核酸 |
| 亲水作用(HILIC) | 极性键合相 | 亲水性分配 | 极性药物、糖类 |
| 尺寸排阻(SEC) | 多孔凝胶 | 分子大小筛选 | 蛋白质、聚合物 |
| 亲和色谱 | 抗体/配体固定相 | 生物特异性 | 蛋白质纯化 |
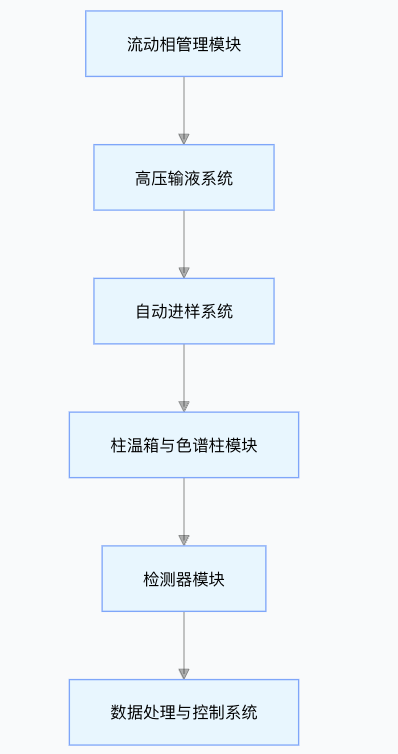
5. 仪器系统组成
5.1 现代HPLC系统架构
5.2 各组件功能
| 组件 | 功能 | 关键指标 |
|---|---|---|
| 输液系统 | 存放流动相 | 脱气处理,避免气泡 |
| 高压泵 | 驱动流动相通过柱 | 压力范围(通常150-600 bar)、流速精度 |
| 进样系统 | 将样品引入系统 | 进样体积精度(0.1-100 μL) |
| 色谱柱 | 分离核心 | 柱长、内径、填料类型、粒径 |
| 检测器 | 检测流出组分 | 紫外(UV)、荧光、蒸发光散射(ELSD)等 |
| 数据系统 | 记录处理信号 | 采集速率、数据存储 |
5.3 经典柱色谱 vs 现代HPLC
| 对比项 | 经典柱色谱 | 现代HPLC |
|---|---|---|
| 驱动方式 | 重力 | 高压泵 |
| 柱压 | 常压~低压 | 中压~高压(可达1000+ bar) |
| 柱效 | 较低 | 极高(数万塔板/米) |
| 分离时间 | 小时~天 | 分钟 |
| 自动化 | 手动 | 全自动 |
| 应用场景 | 教学、简单制备 | 分析、制备、过程控制 |
6. 一个实践案例:理解分离过程
案例:用硅胶柱分离三种染料
背景:使用正相硅胶柱分离偶氮苯(AB)、对甲氧基偶氮苯(MAB)和苏丹黄(SG)
操作:
- 装填活性I级硅胶柱
- 点样:三种染料混合物点在柱顶
- 洗脱:正己烷/乙酸乙酯混合溶剂
- 收集:分步收集流出液
结果观察:
染料颜色带在柱中的迁移:
图片来源于:Sorbtech《Liquid Chromatography Handbook for Classical Column Applications》
柱顶 ────────────────────────── 柱底
│
│ ████ AB (黄色) ← 最先洗脱(极性最低)
│
│ ████ MAB (橙色)
│
│ ████ SG (红色) ← 最后洗脱(极性最高)
│
▼
溶剂前沿
分析:极性吸附原理的应用
- AB极性最低,与硅胶亲和力最弱 → 最先流出
- SG极性最高,与硅胶亲和力最强 → 最后流出
使用标准化的硅胶填料(如Sorbtech Silica Gel, Activity I)可确保批次间一致性,避免分离条件偏移。
7. 本篇要点总结
- 液相色谱 = 固定相 + 流动相 + 分离机制
- 分离源于不同分子在两相间分配差异
- 保留时间 = 定性依据
- 分辨率Rs ≥ 1.5 = 真正的基线分离
- 正相 vs 反相:极性选择方向相反
- 标准化填料 = 可重复分离的保障
问题与讨论
- 你的实验室目前使用哪种色谱模式最多?
- 分离中最常遇到的问题是什么(拖尾、峰展宽、分离度不够?)
参考资料:
Sorbtech《Liquid Chromatography Handbook for Classical Column Applications》