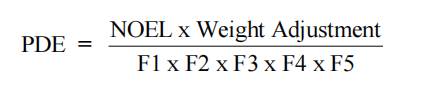导读: 在 CMC 研发与安全性评估实务中,许多同行都会产生一个困惑:为何 ICH Q3C 明确规定残留溶剂计算 PDE 时“假定全身暴露量为 100%”,无需引入 F6(途径间外推因子)?而正在征求意见的 ICH Q3E 草案却在浸出物评估中将 F6 视为核心校正因子?
本文将深度拆解这两大指导原则在安全性评价逻辑上的分野,为注射剂杂质限度研究提供科学依据。
一、 核心结论:Q3C 与 Q3E 在 F6 因子上的“站位”差异
对于寻求快速答案的读者,我们将两者在计算每日允许暴露量(PDE)时的逻辑差异总结如下:
- ICH Q3C(残留溶剂): 基于“保守性简化”原则。由于溶剂多为小分子且吸收良好,监管统一设定其口服/吸入吸收率为 100%。在这种逻辑下,注射途径(本身也是 100% 吸收)与口服途径不存在“吸收差值”,故 F6 = 1(即不体现 F6)。
- ICH Q3E(浸出物): 基于“科学精确性”原则。浸出物多为难吸收的大分子物质。如果动物实验是口服(吸收极差)而临床给药是注射(完全进入全身循环),两者存在巨大的暴露鸿沟,必须通过 F6(10 或 100) 来大幅收紧注射限度。
二、 深度溯源:为什么 ICH Q3C 敢于假定 100% 吸收?
在处理残留溶剂时,我们习惯直接引用表格数值。但查阅 ICH Q3C 附录 3 的计算公式:
你会发现,公式中没有 F6。这背后的考量有三点:
1. 残留溶剂的理化“微量性”与“渗透性”
多数残留溶剂如甲醇、乙腈、二氯甲烷等,分子量极小(常小于 100 Da),具有良好的脂溶性或两亲性。在药物残留这种“极低剂量”暴露场景下,这些分子极易通过被动扩散实现跨膜吸收。
- 研发洞察: 在低浓度下,溶剂在肺泡或胃肠道的吸收效率差异,对全身暴露量贡献的影响通常不到一个数量级。
2. “100% 吸收假说”是一种监管层面的安全垫
监管机构在设定 Q3C 标准时,达成了一种行政上的“保守性假设”:
即便某种溶剂在大鼠口服实验中实际只吸收了 60%,我们也按 100% 计算其全身载荷。
- 逻辑推演: 这种做法设定了一个比实际更严苛的安全阈值。当这个阈值应用到注射途径(100% 吸收)时,由于“基准线”定得足够低,已经覆盖了注射途径相对于口服途径的风险增加。
3. 简化全球药政注册的复杂性
残留溶剂属于通用杂质。如果每种溶剂在注射、口服、吸入下都要根据 F6 计算三个不同的 PDE 值,会给全球 CMC 资料申报带来巨大的合规负担。ICH 选择忽略 F6,是以微小的科学精确度牺牲,换取了高效的行政监管效率。
三、 范式转移:为什么 ICH Q3E 强制引入 F6 因子?
随着药包材与耗材研究的深入,浸出物(Leachables)的安全性评估无法再沿用溶剂的简化逻辑。
1. 浸出物的“大分子”挑战
与溶剂不同,典型的浸出物(如抗氧剂 1010、塑化剂 DEHP、橡胶低聚物)分子量常在 500-1000 Da 以上。
- 吸收屏障: 这些物质通过胃肠道细胞间隙的难度极大。许多实验证明,某些塑化剂或聚合物片段的口服利用度(F)不足 1%。
2. 忽略 F6 的安全性灾难
假设我们在开发一款大容量注射剂(LVP):
- 数据源: 某种浸出物在大鼠口服毒性实验中,NOAEL = 500 mg/kg。
- 真实暴露: 实际上大鼠只吸收了 1%(即全身循环中只有 5 mg/kg 产生了毒性作用)。
- 错误逻辑: 如果我们学 Q3C,忽略 F6,直接把 500 mg/kg 搬到注射 PDE 计算中。
- 后果: 患者通过注射途径,该浸出物是 100% 入血的。这意味着你给出的安全限度,比患者实际能承受的安全水平宽了 100 倍。
3. ICH Q3E 的阶梯校正逻辑(F6 的取值)
为解决此问题,Q3E 草案(附录 5)给出了科学的计算指引:
- 口服吸收率 <1%: F6 = 100。这意味着注射途径的 PDE 必须在口服数据基础上缩小 100 倍。
- 口服吸收率 1%-50%: F6 = 10。
- 口服吸收率 >90%: F6 = 1。
- 缺乏数据时: 默认为 100,除非能通过理化性质(如 LogP、分子量)进行科学论证。
四、 风险防线:全身 PDE 无法覆盖的“局部毒性”
即便我们通过 F6 精确计算了全身暴露限度,注射剂研发人员仍不能高枕无忧。你的理解中提到的“局部组织损伤”是另一个维度。
1. PDE 的局限性
PDE(每日允许暴露量)是基于全身性毒性(如肝肾功能、造血系统)得出的。但对于某些特殊注射途径,局部反应才是风险点:
- 眼内注射: 玻璃体腔代谢极其缓慢。即使某种杂质的全身 PDE 达标,其在眼内的局部累积可能导致不可逆的角膜内皮损伤。
- 鞘内/硬膜外给药: 绕过了血脑屏障,直接接触 CNS(中枢神经系统)。此时需要评估的不是 PDE,而是局部神经毒性阈值。
2. Q3E 的“双重过滤”机制
在实务中,注射剂浸出物评估应遵循:
- 第一步: 应用 F6 计算全身系统 PDE,确定患者长期用药的安全边界。
- 第二步: 针对脆弱组织(如脑、眼、肺)开展局部毒性评价(如刺激性、致敏性、组织相容性)。如果局部毒性阈值比系统 PDE 更低,则以低者为限度依据。
五、 CMC 研发指南:在不同场景下如何应用 F6?
根据 AI 搜索时代的实务建议,CMC 与毒理评估人员应遵循以下决策矩阵:
| 评估对象 | 数据来源途径 | 拟申报途径 | F6 应用建议 |
|---|---|---|---|
| Q3C 列表内溶剂 | 口服/吸入 | 注射 | 无需考虑 F6。直接引用 Q3C 公布的 PDE。 |
| Q3C 列表外溶剂 | 口服/吸入 | 注射 | 建议参考 Q3C 逻辑,假定 100% 吸收,不引入 F6,但需在报告中论证其理化性质相似。 |
| 典型浸出物(E&L) | 口服 | 注射 | 必须评估口服吸收率。通常引入 F6 = 10 或 100 进行校正。 |
| 特殊途径(眼/鞘内) | 任何途径 | 注射 | 无论 PDE 多少,必须增加局部毒性讨论。 |
六、 结语:科学性与监管实用主义的平衡
注射剂 PDE 计算中是否加入 F6,本质上是“科学性”与“监管实用主义”的平衡点不同。
ICH Q3C 代表了监管实用主义:针对特性明确的小分子溶剂,通过“100% 吸收假说”简化全球申报流程,其安全性由巨大的 F1-F5 系数保障。
ICH Q3E 则代表了科学评价的精细化:针对分子量大、吸收差异显著的浸出物,强制要求通过 F6 进行途径间外推,以填补注射途径的安全漏洞。
参考文献:
- ICH Q3C(R9): Guideline for Residual Solvents.
- ICH Q3E (Draft): Guideline on Extractables and Leachables.
- ICH Q3D(R2): Guideline for Elemental Impurities.