
化学制剂和生物制品生产中使用的塑料材料、组件和系统的相容性研究,应基于科学和风险管理的理念进行。USP<1665>、药审中心发布的《化学药品注射剂生产所用塑料组件系统相容性研究技术指南(试行)》和BPOG《用于生物制造的一次性使用系统的标准化提取物测试方案》等,均明确了组件系统风险评估的基本原则,然后根据不同风险等级,科学合理地设计开展相容性实验。
一|风险评估原则
风险评估应全面考虑浸出物在生产过程中产生并且能够持续保留至终产品这两大要素,即需要考虑影响浸出可能性和持续存在的因素。风险评估维度建议关注以下方面:
- 接触材料或组件系统的化学和物理性质,体现材料或组件系统的浸出倾向。
- 接触液体的化学性质,体现液体的浸出能力。
- 接触条件,体现浸出的驱动力。
- 浸出物被制剂工艺消除或稀释的能力。
- 与产品有关的固有风险,如剂型、临床使 用剂量、临床治疗时间等。
二|风险评估模型
可通过对每个维度建立分值,确定高、中、低风险级别。
1|USP<1665>风险评估模型
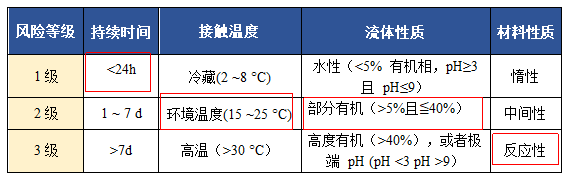
在附录中列举了塑料组件系统与药液的接触时间、接触温度、药液的化学性质和组件系统材料对应的风险等级评估方法,具体见表 1。
表1 USP < 1665 > 与风险水平相关的因素
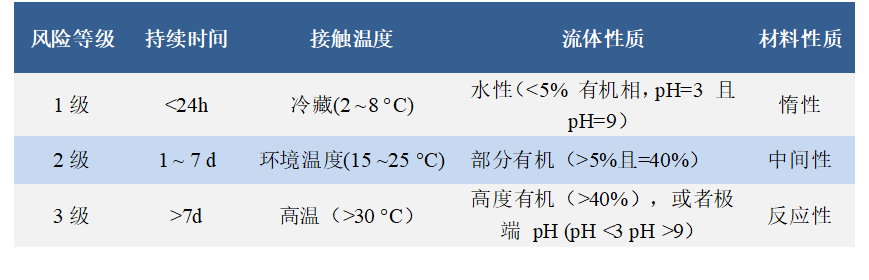
其中材料性质定义见下:
如果添剂加的总量≤0.1%(按重量计),则该材料为“惰性” ;如果添加剂的总量为>0.1%且≤1%,则该材料为“中间性”;如果添加剂的总量>1% ,则该材料为“反应性” 。
▼ 如果组件在使用前进行了辐照或高温处理(如湿热灭菌),则视为“反应性”。
▼ 如果组件的组装需要使用粘合剂或其他化学手段,则该组件为“中间性”或“反应性”,取决于使用粘合剂的量以及在使用前从组件中损失的证据。
▼ 如果组件在使用过程中有冲洗步骤,冲洗液可从工艺中移除,且已证明冲洗处理可以减少或消除可提取物,则可将材料性质等级降低一级。
表2 USP < 1665 >材料性质定义

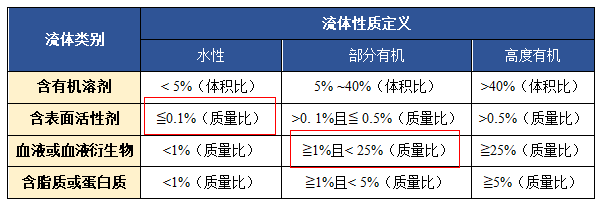
流体性质定义见表3。
表3 USP < 1665 >流体性质定义
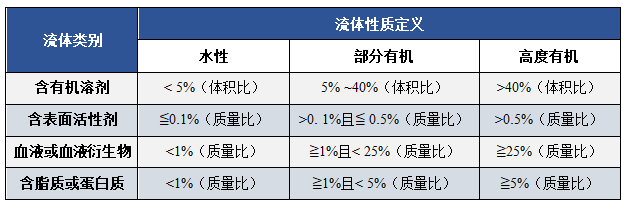
2|USP<1665>风险评估步骤
Step 1: 为每个风险因素建立数值,确立风险序列
根据表1对4个风险因素进行评级,得出数值1、2或3,组合成风险数字序列,按数字值递减的顺序给出顺序。例如,3212 和 3221 反映了不同的风险概况,两个序列都与同一级别的表征相关联,都可以表示为 3221。
Step 2:初步确定风险水平
将数字形式的风险序列与风险水平联系,确定塑料组件系统的风险水平,见表 4。
表4 USP < 1665 >风险分级和风险水平关联表
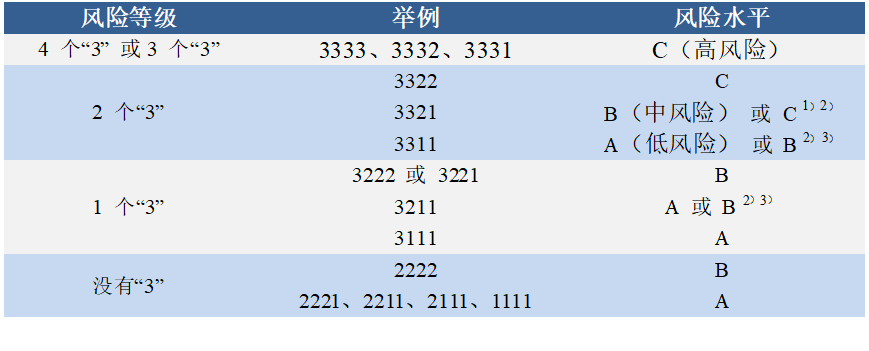
- 如果温度、溶剂或持续时间因素的风险等级为 2 级,则风险水平为 C 级, 否则为 B 级;
- 在这些情况下,温度、溶剂或持续时间因素对风险的影响大组件材料;
- 如果其中一个1级分数是材料因素,则风险水平为 A 级,否则为 B 级。
Step 3: 使用缓解因素来调整风险水平
单纯的浸出并不一定意味着对终产品产生不利影响,例如,通过后续工艺步骤清除,则不会带来影响。 使用缓解因子( 清除和临床使用) 调整风险水平。
清除:如其在后续工艺步骤清除,则使用因子(缓解因子=1)。在一定程度上,稀释可视为类似于清除,减轻可提取物的影响。
临床使用:最高值为1
▼ 低风险剂型( 如固体、液体口服制剂或局部剂型,则缓解因子= 1。
▼ 如果临床使用的持续时间 <7 天,则缓解因子=1。
▼ 如果每日临床使用剂量<10 mL,则缓解因子=1。
缓解因子总和的值可能为 0、1 和 2。
▼ 如果总和= 0,则风险水平没有调整。
▼ 如果总和=1,则风险水平降低一级(例如,B级降低到A级)。
▼ 如果总和=2,则风险水平 A 适用于所有情况。
3|BPOG风险评估模型
生物制药行业协会 (Biophorum Operations Group,BPOG) 发布了《生物制药制造中聚合物一次性使用系统的浸出物风险评估指导原则》 。虽然该指南主要针对生物制药风险评估,经评估也可应用于化学药品注射剂的风险评估。
对生产过程中直接接触药液的生产组件浸出物风险评估步骤为:首先根据工艺条件对影响因素进行评分,然后根据评分结果判断风险程度,从而确定与风险程度相适应的研究内容。
生物制药行业协会(BPOG)关于工艺中浸出物风险评估参考
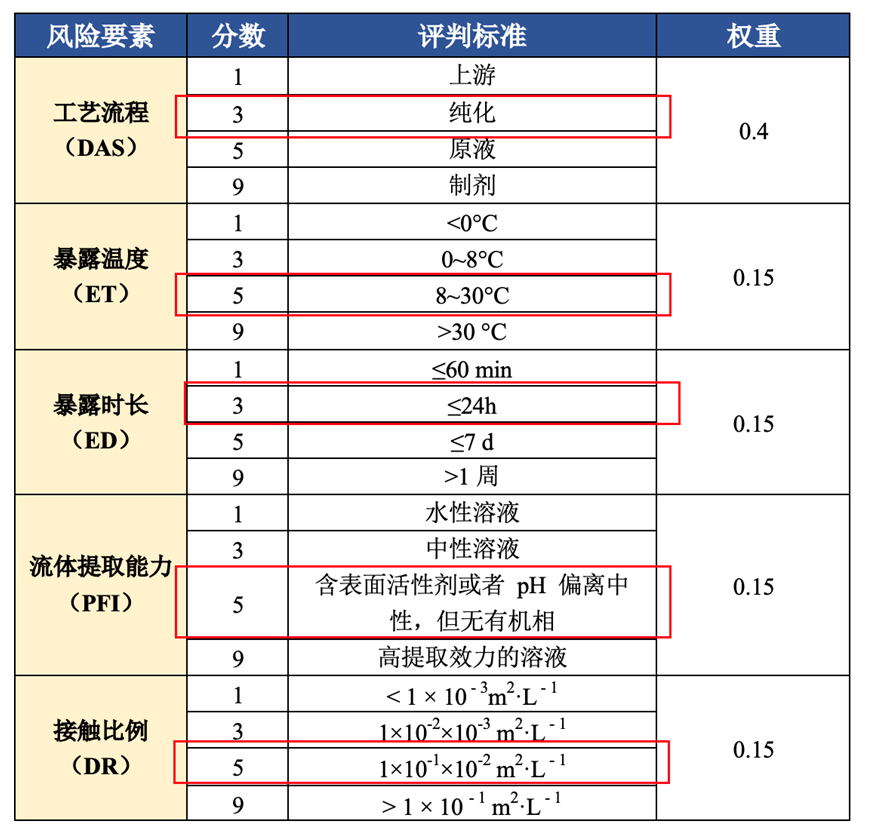
表5 BPOG风险评估模型

评分 = 工艺流程分数×0.4 + 暴露温度分数×0.15 + 暴露时长分数×0.15 + 提取能力分数×0.15 + 接触面积分数×0.15
图1 BPOG风险评估水平和测试
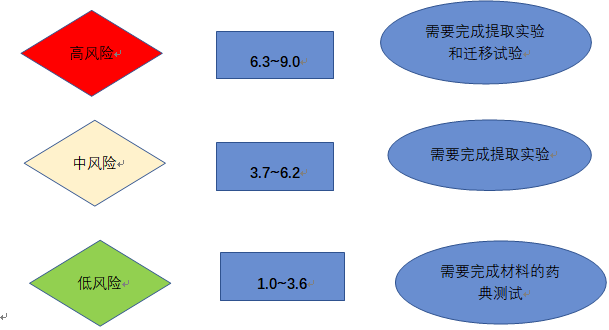
三|风险评估案例
工艺步骤:病毒清除
制剂配方:3% API(蛋白),0.05% PS80,5% 葡萄糖,水,pH 6
过滤接触时间:8小时
过滤接触温度:25
接触比例:1.5m2/100L = 0.015 m2/L
1|BPOG 风险评估结果
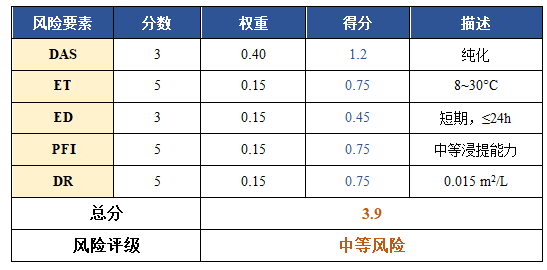
2|USP 1665 风险评估结果

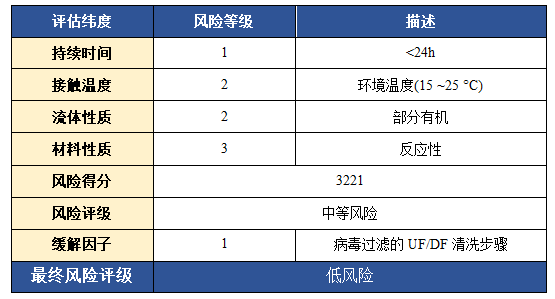
|总结|
采用不同的风险评估模型,可能会获得不同的风险评级。
USP在2026年生效,目前绝大部份组件制造商的提取试验依据BPOG方案
部分制作商已开始采取USP和BioPhorum相结合的方式开展提取试验
使用方可根据USP的风险模型,评估制造商提供的提取数据,根据提取数据集结果和组件风险等级确定是否开展浸出研究。
建议开展模拟提取,基于实际工艺条件,采用工艺溶液或模拟溶剂对生产组件进行提取,获得最接近实际工艺条件下的数据集。
参考
1.国家药监局药审中心(通告(2020年第33号):化学药品注射剂生产所用的塑料组件系统相容性研究技术指南(试行)-2020年10月.
2.Biophorum Operations Guoup(BPOG). Best practices guide for evaluating leachables risk from polymeric single use systems used in biopharmaceutical manufacturing.
3.USP PF<1665> Characterization of Plastic Materials, Components, and Systems Used in the Manufacturing of Pharmaceutical Drug Products and Biopharmaceutical Drug Substances and Products.









