2024年4月6日
2024年4月6日
2024年4月6日
2024年4月6日
2024年4月6日
2024年4月6日
2024年4月5日
2024年3月22日
2024年3月22日
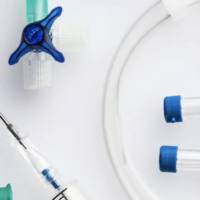
眼科药物的包装思考(监管视角和要求)
本文从监管机构的视角探讨了眼科药物包装材料的安全性和相容性要求。国际和地区监管指南如FDA和EMA设定了严格的标准,包括对包装材料潜在浸出物进行全面评估、化学与毒理学数据提交以及长期稳定性研究。制药公司在药品开发过程中需遵循这些指导进行严谨的风险管理,并在审批阶段面临如何准确执行和解释监管要求的挑战,同时随着科学证据和监管环境的变化不断更新其相容性评估策略。
2024年3月22日
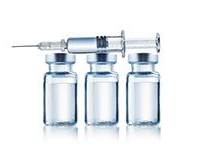
眼科药物的包装思考(应对策略)
本文提出了针对包装材料相容性挑战的应对策略,助力制药企业确保药品安全有效并在全球市场中保持竞争力。这些策略涉及科学的包装材料选择,包括基于材料性质、药品相互作用评估以及对储存条件耐受性的考察;相容性研究方法和最佳实践,如提取物和浸出物研究结合毒理学评估;严格的质量控制和风险管理,包括供应商审计、包装性能监控以及风险评估框架的建立;与监管机构的有效沟通与合作,适应不断更新的监管要求;以及持续的知识管理和培训。这些综合策略的应用,有利于提升药品质量和安全性,驱动包装技术创新,并为企业面对未来的挑战做好准备。